题目内容
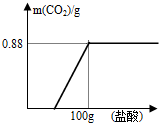 有一瓶因保存不当而部分变质的氢氧化钠固体,为测定其成分,称取10g样品配成溶液,向其中滴加溶质质量分数为7.3%的稀盐酸,放出二氧化碳气体的质量的与加入稀盐酸的质量关系如图所示.试求:
有一瓶因保存不当而部分变质的氢氧化钠固体,为测定其成分,称取10g样品配成溶液,向其中滴加溶质质量分数为7.3%的稀盐酸,放出二氧化碳气体的质量的与加入稀盐酸的质量关系如图所示.试求:(1)样品完全反应后生成二氧化碳
(2)样品中氢氧化钠的质量分数是多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)根据分析图象可知,二氧化碳的最大质量是0.88克进行解答;
(2)写出化学方程式并代入数据计算出碳酸钠的质量,进而求出样品中氢氧化钠的质量以及样品中氢氧化钠的质量分数即可.
(2)写出化学方程式并代入数据计算出碳酸钠的质量,进而求出样品中氢氧化钠的质量以及样品中氢氧化钠的质量分数即可.
解答:解:(1)分析图象可知,二氧化碳的最大质量是0.88g;故填:0.88g;
(2)设生成0.88克二氧化碳消耗的盐酸的质量为x
Na2CO3+2HCl═2NaCl+H2O+CO2↑
73 44
x 0.88g
=
x=1.46g
反应中一共消耗了100g盐酸,所以与氢氧化钠反应的盐酸的质量为:100g×7.3%-1.46g=5.84g
设氢氧化钠的质量为m,
NaOH+HCl═NaCl+H2O
40 36.5
m 5.84g
=
解得:m=6.4g
10g样品中氢氧化钠的质量分数为
×100%=64%
答:样品中氢氧化钠的质量分数是64%.
(2)设生成0.88克二氧化碳消耗的盐酸的质量为x
Na2CO3+2HCl═2NaCl+H2O+CO2↑
73 44
x 0.88g
| 73 |
| x |
| 44 |
| 0.88g |
x=1.46g
反应中一共消耗了100g盐酸,所以与氢氧化钠反应的盐酸的质量为:100g×7.3%-1.46g=5.84g
设氢氧化钠的质量为m,
NaOH+HCl═NaCl+H2O
40 36.5
m 5.84g
| 40 |
| m |
| 36.5 |
| 5.84g |
解得:m=6.4g
10g样品中氢氧化钠的质量分数为
| 6.4g |
| 10g |
答:样品中氢氧化钠的质量分数是64%.
点评:培养学生分析图形的能力,掌握化学计算的格式和规范性.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
下列符号既表示一种元素,又能表示一个原子,还能表示一种物质的是( )
| A、H2 | B、2Mg |
| C、N | D、Hg |
大蒜是常见的调味品之一,大蒜中主要成分大蒜素具有消毒杀菌作用.大蒜素的化学式为C6H10S3,下列说法不正确的是( )
| A、大蒜素的一个分子由6个碳原子、10个氢原子和3个硫原子构成 |
| B、大蒜素由碳、氢、硫三种元素组成 |
| C、大蒜素中碳、氢、硫三种元素的质量比为6:10:3 |
| D、大蒜素的相对分子质量的计算式为:12×6+1×10+32×3 |
下列关于硝基苯(C6H5NO2)的说法正确的是( )
| A、硝基苯是氧化物 |
| B、硝基苯由碳、氢、氧、氮四种元素组成 |
| C、硝基苯分子由14个原子构成 |
| D、硝基苯的相对分子质量是122 |
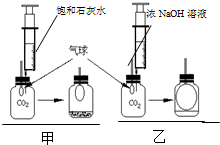 浓NaOH溶液
浓NaOH溶液