题目内容
某元素A最外层有3个电子,其氧化物中氧元素与A元素质量比8:9,求A的相对原子质量.
考点:元素质量比的计算
专题:化学式的计算
分析:根据题意,某元素A最外层有3个电子,在发生化学反应时容易失去3个电子形成带3个单位正电荷的阳离子,化合价的数值等于离子所带电荷的数值,且符号一致;则A元素的化合价为+3价;氧元素显-2价,则A元素氧化物的化学式为A2O3,据此结合化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
解答:解:某元素A最外层有3个电子,在发生化学反应时容易失去3个电子形成带3个单位正电荷的阳离子,化合价的数值等于离子所带电荷的数值,且符号一致;则A元素的化合价为+3价;氧元素显-2价,则A元素氧化物的化学式为A2O3,其氧化物中氧元素与A元素质量比8:9,设A原子的相对原子质量为x,则(16×3):2x=8:9,x=27.
答:A的相对原子质量为27.
答:A的相对原子质量为27.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列有关催化剂的叙述中,正确的是( )
| A、二氧化锰用够用于所有反应的催化剂 |
| B、在过氧化氢分解前后,二氧化锰的质量和化学性质均未改变 |
| C、催化剂一定能够加快化学反应速率 |
| D、加热氯酸钾时如果不加入催化剂则无法获得氧气 |
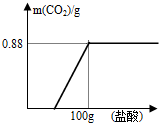 有一瓶因保存不当而部分变质的氢氧化钠固体,为测定其成分,称取10g样品配成溶液,向其中滴加溶质质量分数为7.3%的稀盐酸,放出二氧化碳气体的质量的与加入稀盐酸的质量关系如图所示.试求:
有一瓶因保存不当而部分变质的氢氧化钠固体,为测定其成分,称取10g样品配成溶液,向其中滴加溶质质量分数为7.3%的稀盐酸,放出二氧化碳气体的质量的与加入稀盐酸的质量关系如图所示.试求:
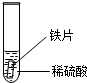
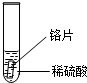
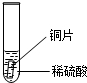
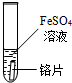

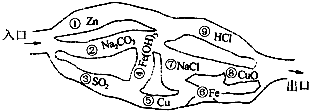 “探险队员”--硫酸,不小心走进了有许多“吃人的野兽”(即能与硫酸发生化学反应的物质)的小山,请你帮助它走出小山.请用图中物质间的序号连接起来表示所走的路线:入口→
“探险队员”--硫酸,不小心走进了有许多“吃人的野兽”(即能与硫酸发生化学反应的物质)的小山,请你帮助它走出小山.请用图中物质间的序号连接起来表示所走的路线:入口→