题目内容
1. 在实验室中,常用过氧化氢溶液与二氧化锰的混合物制取氧气.
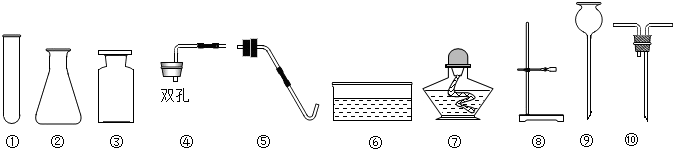
在实验室中,常用过氧化氢溶液与二氧化锰的混合物制取氧气.(1)请写出标号仪器名称:①铁架台
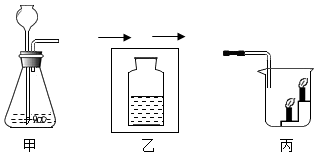
(2)请写出实验室用分解过氧化氢的方法制取氧气的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;制取装置如图所示,可用如图所示方法收集氧气的原因是氧气的密度比空气大.反应后二氧锰的质量不变(填“增大”、“减小”或“不变”)
(3)如果锥形瓶中的反应很剧烈,若要减慢反应速率,下列措施可行的是A
A.减慢液体的滴加速度 B.换用体积较小的锥形瓶 C.加热锥形瓶
(4)实验室常用大理石和稀盐酸在常温下反应制取CO2气体,实验室能(填“能”或“不能”)用此装置制取CO2气体.写出实验室制取CO2的方程式CaCO3+2HCl═CaCl2+H2O+CO2↑,检验二氧化碳的试剂是澄清石灰水.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据过氧化氢在二氧化锰的催化作用下分解生成水和氧气,如图所示方法收集氧气的方法是向上排空气法,二氧化锰是该反应的催化剂进行分析;
(3)根据影响反应速率的因素进行分析;
(4)根据实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,实验室检验二氧化碳的试剂是澄清石灰水进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,①是铁架台;
(2)过氧化氢在二氧化锰的催化作用下分解生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,如图所示方法收集氧气的方法是向上排空气法,原因是:氧气的密度比空气大,二氧化锰是该反应的催化剂,所以反应后二氧锰的质量不变;
(3)减慢液体的滴加速度,可以减慢反应速率;换用体积较小的锥形瓶,会使反应反应更剧烈,甚至爆炸;加热锥形瓶,会加快反应速率,故选:A;
(4)实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,所以实验室能用此装置制取CO2气体,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑,实验室检验二氧化碳的试剂是澄清石灰水.
故答案为:(1)铁架台;
(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,氧气的密度比空气大,不变;
(3)A;
(4)能,CaCO3+2HCl═CaCl2+H2O+CO2↑,澄清石灰水.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案①颜色 ②状态 ③密度 ④导电性 ⑤可燃性 ⑥硬度 ⑦易生锈 ⑧溶解性.
| A. | ①④⑤ | B. | ①②③④⑧ | C. | ①②④⑥⑦⑧ | D. | ①②③④⑥⑧ |
| A. | FeCl3 | B. | BaCl2 | C. | CO2 | D. | KOH |
 石墨烯是“新材料之王”
石墨烯是“新材料之王”