题目内容
12. 科学家用点燃氢气的,验证燃烧产物的方法,证实了水的组成.
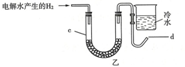
科学家用点燃氢气的,验证燃烧产物的方法,证实了水的组成.(1)如果将电解水长生的氢气直接缓缓地通过装有足量无水硫酸铜的仪器c,并在导管口b处点燃,然后把盛有冷水的烧杯置于如图所示的位置,实验过程中可以观察到的现象是无水硫酸铜变蓝;导管d处有淡蓝色火焰;烧杯底部附着着小水珠.d处发生反应的化学方程式为2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
(2)在进行电解水的实验时,常加入少量NaOH以增强水的导电性,NaOH不被电解.若将质量分数为5%的NaOH溶液100g进行电解,当溶液中NaOH的质量分数改变了1%时停止电解,则生成H2的质量约为1.9g.
分析 (1)根据用无水硫酸铜检验并除去气体中少量的水,然后点燃氢气生成水进行解答;
(2)根据电解水时,氢氧化钠的质量不变、质量分数增加进行计算.
解答 解:(1)实验过程为用无水硫酸铜检验并除去气体中少量的水,然后点燃气体,氢气燃烧生成的水遇温度较低烧杯,在杯底凝结成液态水;所以观察到的现象是:无水硫酸铜变蓝;导管d处有淡蓝色火焰;烧杯底部附着着小水珠;d处发生反应的化学方程式为2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;
故答案为:无水硫酸铜变蓝;导管d处有淡蓝色火焰;烧杯底部附着着小水珠;2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;
(2)加入少量氢氧化钠是为了增强水的导电性,反应前后其质量保持不变,随着电解水实验的进行,水的质量不断减少,则其溶质的质量分数不断增加,现在溶液中NaOH的质量分数改变了1%,说明变为6%,设现在溶液的质量为X,则有100g×5%=X×6%,解得X≈83.3g,则电解水的质量是100g-83.3g=16.7g,电解水生成氢气和氧气,可知生成H2的质量等于水中氢元素的质量,为:16.7g×$\frac{2}{18}$×100%≈1.9g.
故填:1.9.
点评 无水硫酸铜为白色粉末,遇水可生成蓝色硫酸铜晶体,常用此白色粉末检验水的存在.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.实验室用高锰酸钾制氧气时,不需要使用的仪器是( )
| A. |  | B. |  | C. |  | D. |  |
3.大蒜中含有一种有效成分辣素“硫化丙烯”,其化学式为C3H6S,能杀菌,具有一定的抗病功能和食疗价值.下列关于硫化丙烯的说法中正确的是( )
| A. | 1个硫化丙烯分子中含有3个氢分子 | |
| B. | 硫化丙烯由三个碳元素、六个氢元素、一个氧元素组成 | |
| C. | 硫化丙烯分子由碳、氢、氧三种元素组成 | |
| D. | 1个硫化丙烯分子由3个碳原子、6个氢原子、1个硫原子构成 |
20.某化学反应中,各物质质量(m)随时间(t)变化的曲线如图所示.下列说法正确的是( )


| A. | 该反应是化合反应 | |
| B. | 甲一定是该反应的催化剂 | |
| C. | 乙、丙可能是单质,丁可能是化合物 | |
| D. | t1时丁的质量等于乙、丙的质量之和 |
7.水是很好的溶剂.下表列出了氯化铵和氯化钠在水中的溶解度,回答下列问题.
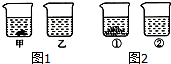
(1)40℃时,向两个分别盛有45gNH4Cl和NaCl的烧杯中,各加人100g的水,充分溶解后,结果如图1所示,则乙烧杯中的溶质是NH4Cl.
(2)采用一种操作方法,将上述的不饱和溶液变为饱和溶液.下列说法正确的是C(填字母序号,下同).
A.溶质的质量一定不变
B.溶液中溶质的质量分数一定增大
C.溶液质量可能不变
D.可升高温度或减少溶剂
(3)采用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液.下列说法正确的是BC.
A.溶剂质量可能不变
B.溶液中溶质的质量分数一定减小
C.溶液质量一定增大
D.溶液中溶质的质量分数可能增大
(4)30℃时,向两个分别盛有相同质量的氯化钠和氯化铵的烧杯中,各加人100g水,充分溶解后,恢复至30℃,其结果如图2所示. 有关下列说法中,正确的是BD.
A.烧杯②中溶液是不饱和溶液
B.升高温度或增加溶剂都有可能将烧杯①中固体全部溶解
C.若将烧杯①中的溶液变为不饱和溶液,溶液中溶质质量分数一定减小
D.将得到的烧杯②中溶液降温至0℃时,溶液中溶质质量分数一定减小.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |

(2)采用一种操作方法,将上述的不饱和溶液变为饱和溶液.下列说法正确的是C(填字母序号,下同).
A.溶质的质量一定不变
B.溶液中溶质的质量分数一定增大
C.溶液质量可能不变
D.可升高温度或减少溶剂
(3)采用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液.下列说法正确的是BC.
A.溶剂质量可能不变
B.溶液中溶质的质量分数一定减小
C.溶液质量一定增大
D.溶液中溶质的质量分数可能增大
(4)30℃时,向两个分别盛有相同质量的氯化钠和氯化铵的烧杯中,各加人100g水,充分溶解后,恢复至30℃,其结果如图2所示. 有关下列说法中,正确的是BD.
A.烧杯②中溶液是不饱和溶液
B.升高温度或增加溶剂都有可能将烧杯①中固体全部溶解
C.若将烧杯①中的溶液变为不饱和溶液,溶液中溶质质量分数一定减小
D.将得到的烧杯②中溶液降温至0℃时,溶液中溶质质量分数一定减小.
4.括号内是区别下列各组物质的试剂方法,其中错误的是( )
| A. | 氯化钙溶液与蒸馏水(肥皂水,振荡) | |
| B. | 水与过氧化氢溶液(加入少量二氧化锰) | |
| C. | 二氧化碳和氮气(燃着的木条) | |
| D. | 食盐水和蒸馏水(蒸发) |


 ,请回答下列问题:
,请回答下列问题: ;写出实验室用X2Y2制氧气的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
;写出实验室用X2Y2制氧气的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.