题目内容
1.亚硝酸钠是一种工业用盐,外形与食盐相似,它有毒、有咸味.人若误食会危害人体健康,引起中毒,甚至致人死亡.亚硝酸钠的水溶液呈碱性,食盐的水溶液呈中性.请你设计实验鉴别亚硝酸钠和食盐.分析 鉴别物质时,首先对需要鉴别的物质的性质进行对比分析找出特性,再根据性质的不同,选择适当的试剂,出现不同的现象的才能鉴别.
解答 解:根据题意,亚硝酸钠的水溶液呈碱性,食盐的水溶液呈中性,可分别取少量的两种固体于试管中,加入少量的蒸馏水,振荡,分别滴加无色酚酞溶液,能使酚酞溶液变红色的是亚硝酸钠,无明显变化的是氯化钠(合理即可).
故答案为:分别取少量的两种固体于试管中,加入少量的蒸馏水,振荡,分别滴加无色酚酞溶液,能使酚酞溶液变红色的是亚硝酸钠,无明显变化的是氯化钠(合理即可).
点评 本题有一定难度,在解决鉴别物质题时,判断的依据是:所选试剂需要与待鉴别的物质反应并出现明显不同的现象.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案
相关题目
2.Fenton法常用于处理含难降解有机物的工业废水.其原理利用Fe2+和H2O2的反应产生能降解污染物的活性成分.现运用该方法降解有机污染物p-CP,探究有关因素对降解反应速率的影响.
实验探究:控制p-CP的初始浓度相同,实验温度恒定在25℃或40℃(其余实验条件见表),设计如下对比试验.
(1)请完成以下实验设计表(表中不要留空格).
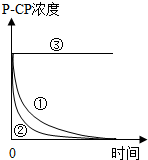
实验测得p-CP的浓度随时间变化的关系如图.
(2)实验①、②表明温度升高,降解反应速率加快.实验发现,温度过高时,降解反应较难发生.请从Fenton法所用试剂H2O2的角度分析原因:过氧化氢在温度过高时易分解.
(3)实验③得出的结论是:pH等于10时,反应速率趋向于零.
(4)为测定不同时间内有机物降解的浓度,需在不同时间从反应器中取样,并使所取样品中的降解反应立即停止下来.根据如图中的信息,给出一种迅速停止反应的方法:将所取样品迅速加入到一定量的NaOH溶液中,使pH为10.
实验探究:控制p-CP的初始浓度相同,实验温度恒定在25℃或40℃(其余实验条件见表),设计如下对比试验.
(1)请完成以下实验设计表(表中不要留空格).
| 实验编号 | 实验目的 | 温度/ | pH | 浓度/(mg.L-1) | |
| ① | 为提供参照 | 25 | 3 | H2O2 | Fe2+ |
| ② | 探究温度对降解反应速率的影响 | 204 | 16.8 | ||
| ③ | 25 | 10 | 204 | 16.8 | |
(2)实验①、②表明温度升高,降解反应速率加快.实验发现,温度过高时,降解反应较难发生.请从Fenton法所用试剂H2O2的角度分析原因:过氧化氢在温度过高时易分解.
(3)实验③得出的结论是:pH等于10时,反应速率趋向于零.
(4)为测定不同时间内有机物降解的浓度,需在不同时间从反应器中取样,并使所取样品中的降解反应立即停止下来.根据如图中的信息,给出一种迅速停止反应的方法:将所取样品迅速加入到一定量的NaOH溶液中,使pH为10.

10.下列实验现象描述错误的是( )
| A. | 硫酸铵和熟石灰在研钵中研磨,闻到有刺激性气味气体 | |
| B. | 电解水时正极产生的气体体积比负极产生的气体体积少 | |
| C. | 硫粉在空气中燃烧,发出淡蓝色火焰,有刺激性气味气体生成 | |
| D. | 红磷在氧气中燃烧,发出明亮的火焰,放热,产生大量的白雾 |
11.化学与生活紧密联系.下列说法正确的是( )
| A. | 二氧化碳是造成酸雨的主要因素 | |
| B. | 用洗洁精洗涤餐具油污属于乳化作用 | |
| C. | 用焚烧的方法处理废弃的塑料制品会造成“白色污染” | |
| D. | 铝合金比铁制品耐腐蚀是因为铝的化学性质不如铁活泼 |
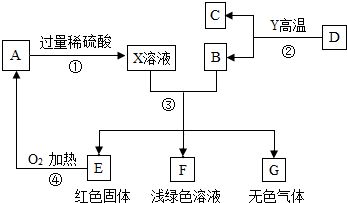 A、B、C、D、E、F、G为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应,它们之间的相互转化关系如下图所示:
A、B、C、D、E、F、G为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应,它们之间的相互转化关系如下图所示: A~G是初中化学常见的7种物质,其中至少有一种是无色气体,其A与G含有相同的金属元素,它们在一定条件下转化关系如图所示,其中部分反应物或生成物和反应条件已略去.
A~G是初中化学常见的7种物质,其中至少有一种是无色气体,其A与G含有相同的金属元素,它们在一定条件下转化关系如图所示,其中部分反应物或生成物和反应条件已略去.