题目内容
19.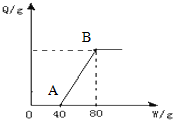 向50g含有氯化氢和氯化铜的混合溶液中加入10%的氢氧化钠溶液,产生沉淀的质量Q与加入氢氧化钠溶液的质量W的关系如图所示,则下列说法不正确的是( )
向50g含有氯化氢和氯化铜的混合溶液中加入10%的氢氧化钠溶液,产生沉淀的质量Q与加入氢氧化钠溶液的质量W的关系如图所示,则下列说法不正确的是( )| A. | B点对应的纵坐标是9.8克 | |
| B. | A点对应溶质只有氯化铜 | |
| C. | OA段发生的反应是中和反应 | |
| D. | B点对应的溶液中含有的氯化钠质量是11.7克 |
分析 A、B点表示恰好完全反应;
B、A点表示氢氧化钠与盐酸恰好反应完,再去考虑溶质是谁;
C、根据OA段发生的反应是氢氧化钠与盐酸中和反应分析;
D、根据B点溶液中的溶质含量分析.
解答 解:A、B点表示氯化铜和氢氧化钠完全反应,
设生成沉淀质量为x,
2NaOH~Cu(OH)2↓
80 98
(80g-40g)×10% x
$\frac{80}{(80g-40g)×10%}=\frac{98}{x}$
x=4.9g;故A错误;
B、A点表示氢氧化钠与盐酸恰好反应完,氯化铜还没参加反应,此时溶质是氯化钠和氯化铜,故B错误;
C、OA段发生的反应是氢氧化钠与盐酸中和反应,正确;
D、B点表示的氯化铜和氢氧化钠恰好完全反应,A点表示氯化铜和氢氧化钠恰好完全反应后,
B点溶液中含有的氯化钠质量为y,
NaOH~NaCl
40 58.5
80g×10% y
$\frac{40}{80g×10%}=\frac{58.5}{y}$
y=11.7g
故D正确.
故选:AB.
点评 本题重点考查复分解反应的实质,学会分析图象,判断产物,属于一道溶液综合性的题目.

练习册系列答案
相关题目
14.下列化学符号只具有微观含义的是( )
| A. | O2 | B. | 2H | C. | Fe | D. | H2O |
10.金属元素R的氧化物化学式为R2O3,若R的化合价不变,则R的下列化合物中化学式正确的是( )
| A. | R(OH)3 | B. | R(NO3)2 | C. | RCl2 | D. | RSO4 |
14.下列物质不能用于鉴别氢氧化钠溶液和稀盐酸的是( )
| A. | 酚酞试液 | B. | CO2 | C. | 氢氧化铜 | D. | 铁粉 |
8.下列实验方案不可行的是( )
| A. | 用肥皂水区分硬水与软水 | B. | 用水区分硝酸铵固体与蔗糖固体 | ||
| C. | 用水溶解以除去衣服上的油污 | D. | 实验室用电解水制取氢气 |