题目内容
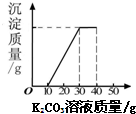 某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40mL该溶液于烧杯中,滴入40g溶质质量分数为13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如右图所示.求:
某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40mL该溶液于烧杯中,滴入40g溶质质量分数为13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如右图所示.求:(1)生成的气体和沉淀的质量.
(2)实验结束后,若将烧杯中的物质蒸干,得到无水固体的质量.
分析:(1)根据碳酸钾会与盐酸反应生成二氧化碳气体,碳酸钾会与氯化钙生成碳酸钙沉淀进行分析,
(2)根据质量守恒定律进行分析.
(2)根据质量守恒定律进行分析.
解答:解:(1)从图象中的数据可以看出,10克之前没有出现沉淀,所以和盐酸反应的碳酸钾溶液的质量是10g,从10开始出现沉淀,到30沉淀不变,说明和氯化钙反应的碳酸钾溶液的质量是20g,根据化学方程式可求得生成气体和沉淀碳酸钙的质量;
设生成氯化钾为x,生成二氧化碳气体的质量为y
K2CO3 +2HCl=2KCl+H2O+CO2↑
138 149 44
10g×13.8% x y
=
=
X=1.49g y=0.44g
设反应生成氯化钾为a,生成的碳酸钙质量b
K2CO3 +CaCl2=2KCl+CaCO3↓
138 149 100
20×13.8% a b
=
=
a=2.98g b=2g
所以生成的二氧化碳气体和碳酸钙沉淀的质量分别为0.44g、2g
(2)反应后烧杯中的物质包括两个反应中生成的氯化钾,以及反应剩余的碳酸钾和生成的沉淀碳酸钙的质量,故得到无水固体的质量为:1.49g+2.98g+10g×13.8%+2g=7.85g.
答:(1)生成的气体和沉淀的质量分别为0.44g、2g.
(2)实验结束后,将烧杯中的物质蒸干,得到无水固体的质量为7.85g.
设生成氯化钾为x,生成二氧化碳气体的质量为y
K2CO3 +2HCl=2KCl+H2O+CO2↑
138 149 44
10g×13.8% x y
| 138 |
| 10g×13.8% |
| 149 |
| x |
| 44 |
| y |
X=1.49g y=0.44g
设反应生成氯化钾为a,生成的碳酸钙质量b
K2CO3 +CaCl2=2KCl+CaCO3↓
138 149 100
20×13.8% a b
| 138 |
| 20g×13.8% |
| 149 |
| a |
| 100 |
| b |
a=2.98g b=2g
所以生成的二氧化碳气体和碳酸钙沉淀的质量分别为0.44g、2g
(2)反应后烧杯中的物质包括两个反应中生成的氯化钾,以及反应剩余的碳酸钾和生成的沉淀碳酸钙的质量,故得到无水固体的质量为:1.49g+2.98g+10g×13.8%+2g=7.85g.
答:(1)生成的气体和沉淀的质量分别为0.44g、2g.
(2)实验结束后,将烧杯中的物质蒸干,得到无水固体的质量为7.85g.
点评:在解此类题时,首先根据图象分析反应的原理,然后再根据题中的条件利用方程式进行求解.最后得到无水固体的质量注意要包含碳酸钙的质量,因为题干要求的是烧杯内的物质.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目
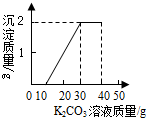 某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40mL该溶液于烧杯中,滴入40g溶质质量分数为13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如图所示.求:
某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40mL该溶液于烧杯中,滴入40g溶质质量分数为13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如图所示.求: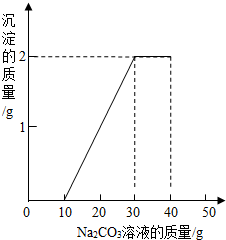 某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合液(不考虑其他杂质)进行如下实验:取一定量该混合液于烧杯中,滴加40g溶质质量分数为10.6%的碳酸钠溶液后,称得烧杯内溶液总质量为68.5g.滴入碳酸钠溶液的质量与生成沉淀质量关系如图所示.
某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合液(不考虑其他杂质)进行如下实验:取一定量该混合液于烧杯中,滴加40g溶质质量分数为10.6%的碳酸钠溶液后,称得烧杯内溶液总质量为68.5g.滴入碳酸钠溶液的质量与生成沉淀质量关系如图所示.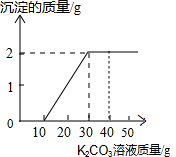 某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40g该溶液于烧杯中,滴入40g溶质质量分数为 13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如如图所示.回答下列问题:(最后结果保留1位小数)
某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40g该溶液于烧杯中,滴入40g溶质质量分数为 13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如如图所示.回答下列问题:(最后结果保留1位小数) (2006?北京)某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40mL该溶液于烧杯中,滴入40g溶质质量分数为13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如图所示.求:
(2006?北京)某班同学完成制取二氧化碳的实验后,对回收的盐酸和氯化钙混合溶液(不考虑其他杂质)进行了以下实验:取40mL该溶液于烧杯中,滴入40g溶质质量分数为13.8%的K2CO3溶液.滴入K2CO3溶液质量与生成沉淀质量的关系如图所示.求: