题目内容
用25克石灰石样品,现取125克稀盐酸平均分成五分,每次加入25克与石灰石样品反应﹙杂质不与稀盐酸反应﹚,反应情况如下表所示:
| 次数 | 1 | 2 | 3 | 4 | 5 |
| 加入稀盐酸的总质量/ | 25 | 50 | 75 | 100 | 125 |
| 容器中剩余物质总质量 | 47.8 | 70.6 | 93.4 | 116.2 | 141.2 |
解:根据质量守恒定律可知,第一次放出二氧化碳的质量=25g+25克-47.8g=2.2g,说明每加入25g盐酸,放出二氧化碳的质量为2.2g;第二次加入50g盐酸后生成二氧化碳的质量=25g+50g-70.6g═4.4gg,因此此时盐酸无剩余;而第三次加入75g盐酸,生成二氧化碳的质量是75g+25g-93.4g=6.6g,此时盐酸也无剩余;第四次实验中生成的二氧化碳质量是25g+100g-116.2g=8.8g;此时盐酸也无剩余;第五次反应生成的二氧化碳质量是25g+125g-141.2g=8.8g,故其中25g盐酸没有参与反应,因此反应最后生成的二氧化碳质量是8.8g;
设样品中碳酸钙的质量是x
设碳酸钙的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 8.8g

x=20g
样品中碳酸钙的质量分数=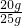 ×100%=80%.
×100%=80%.
答:完全反应后生成二氧化碳的质量是8.8g;石灰石样品中碳酸钙的质量分数为80%.
分析:根据质量守恒定律可知,第一次放出二氧化碳的质量=25g+25g-47.8g=2.2g,说明每加入25g盐酸,放出二氧化碳的质量为2.2g.第二次加入50g盐酸后生成二氧化碳的质量=25g+50g-70.6g═4.4g,因此此时盐酸无剩余.而第三次加入75g盐酸,生成二氧化碳的质量是75g+25g-93.4g=6.6g,此时盐酸也无剩余,继续对4、5次的二氧化碳的质量进行分析即可解答此题;
点评:学会分析表格并从表格中搜索信息的方法,掌握化学方程式的计算格式和规范性是解题的关键.
设样品中碳酸钙的质量是x
设碳酸钙的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 8.8g

x=20g
样品中碳酸钙的质量分数=
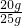 ×100%=80%.
×100%=80%.答:完全反应后生成二氧化碳的质量是8.8g;石灰石样品中碳酸钙的质量分数为80%.
分析:根据质量守恒定律可知,第一次放出二氧化碳的质量=25g+25g-47.8g=2.2g,说明每加入25g盐酸,放出二氧化碳的质量为2.2g.第二次加入50g盐酸后生成二氧化碳的质量=25g+50g-70.6g═4.4g,因此此时盐酸无剩余.而第三次加入75g盐酸,生成二氧化碳的质量是75g+25g-93.4g=6.6g,此时盐酸也无剩余,继续对4、5次的二氧化碳的质量进行分析即可解答此题;
点评:学会分析表格并从表格中搜索信息的方法,掌握化学方程式的计算格式和规范性是解题的关键.

练习册系列答案
相关题目
 请根据下面有关信息,按题目要求回答问题:
请根据下面有关信息,按题目要求回答问题: