题目内容
7.化学是以实验为基础的学科,如图是课本中第八单元的两个实验,据图回答:
(1)上述实验目的是:探究金属活动性顺序;
(2)实验1中发生反应的方程式为2Al+3CuSO4=Al2(SO4)3+3Cu;实验2中的现象铜的表面出现银白色物质,溶液逐渐由无色变为蓝色.
(3)综合两个实验的现象,得出的结论是铝、铜、银的金属活动性依次减弱.
分析 通过实验可以探究金属活动性顺序;
铝能和硫酸铜反应生成硫酸铝和铜,铜能和硝酸银反应生成硝酸铜和银.
解答 解:(1)通过实验1可知铝比铜活泼,通过实验2可知铜比银活泼,因此上述实验目的是探究金属活动性顺序.
故填:探究金属活动性顺序.
(2)实验1中,铝能和硫酸铜反应生成硫酸铝和铜,发生反应的方程式为:2Al+3CuSO4=Al2(SO4)3+3Cu;
实验2中,铜能和硝酸银反应生成硝酸铜和银,实验现象是:铜的表面出现银白色物质,溶液逐渐由无色变为蓝色.
故填:2Al+3CuSO4=Al2(SO4)3+3Cu;铜的表面出现银白色物质,溶液逐渐由无色变为蓝色.
(3)铝能和硫酸铜反应生成硫酸铝和铜,说明铝比铜活泼,铜能和硝酸银反应生成硝酸铜和银,说明铜比银活泼,综合两个实验的现象,得出的结论是铝、铜、银的金属活动性依次减弱.
故填:铝、铜、银的金属活动性依次减弱.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
17.有关碳单质及其氧化物的说法中正确的是( )
| A. | C、CO、CO2都具有还原性 | |
| B. | 一定条件下,石墨转化成金刚石是物理变化 | |
| C. | 用紫色石蕊溶液可区分CO和CO2 | |
| D. | 碳具有可燃性,因此在常温下其化学性质比较活泼 |
18.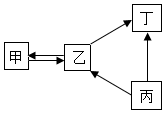 甲、乙、丙、丁均为初中化学常见物质,它们之间的部分转化关系如图所示.下列说法正确的是( )
甲、乙、丙、丁均为初中化学常见物质,它们之间的部分转化关系如图所示.下列说法正确的是( )
 甲、乙、丙、丁均为初中化学常见物质,它们之间的部分转化关系如图所示.下列说法正确的是( )
甲、乙、丙、丁均为初中化学常见物质,它们之间的部分转化关系如图所示.下列说法正确的是( )| A. | 若甲、乙、丁都是氧化物,则丙可能是碳酸钙 | |
| B. | 若丙是碳酸钠,乙是氢氧化钠,则甲可能是硝酸钠 | |
| C. | 若甲、乙、丙、丁均含有同一种元素,且乙可用来灭火,则丙可能是氧气 | |
| D. | 甲、乙、丙、丁之间的转化不可以全部通过复分解反应实现 |
15.除去下列物质中的少量杂质,所选用的试剂、操作方法都正确的是( )
| 选项 | 物质 | 杂质 | 试剂 | 操作方法 |
| A | MnO2 | KCl | 适量水 | 溶解、过滤、洗涤、干燥 |
| B | O2 | H2O | 浓硫酸 | 通过盛有浓硫酸的洗气瓶 |
| C | CaO | CaCO3 | 稀盐酸 | 过滤、蒸发结晶 |
| D | NaOH | Ca(OH)2 | 过量Na2CO3溶液 | 溶解、过滤、蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
2.下列实验操作正确的是( )
| A. | 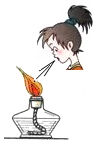 熄灭酒精灯 | B. | 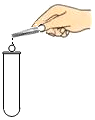 取用大理石块 | C. | 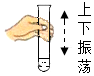 振荡试管 | D. |  闻气味 |
16.下列实验操作错误的是( )
| A. |  氢气还原氧化铜 | B. |  称量药品 称量药品 | C. |  测定溶液pH | D. |  检查气密性 |
17.类推是化学学习中常用的思维方法,以下类推结果中正确的是( )
| A. | 盐中含有金属离子和酸根离子,NH4NO3中没有金属离子,不属于盐类 | |
| B. | 碱的水溶液显碱性,所以NaOH的水溶液一定是碱性溶液 | |
| C. | 酸溶液能使紫色石蕊试液变红,所以能使紫色石蕊试液变红的一定是酸的溶液 | |
| D. | 燃烧一般都伴随发光、放热现象,所以有发光、放热现象的变红就是燃烧 |
 2016年2月4日,国务院发布了《关于钢铁行业化解过剩产能,实现脱困发展的意见》,推动钢铁行业升级.钢铁是一种重要的金属材料.
2016年2月4日,国务院发布了《关于钢铁行业化解过剩产能,实现脱困发展的意见》,推动钢铁行业升级.钢铁是一种重要的金属材料.