��Ŀ����
FeSO4•7H2O��һ����Ҫ��ʳƷ���������Ӽ���ij��ҵ������Ҫ�ɷ���Fe2O3��������CaCO8��SiO2���Ȳ�����ˮҲ������ϡ���ᣩ��ʵ�����ô˷����Ʊ�FeSO4•7H2O��������ͼ1��

���������ͼ�ش��������⣺
��1��ϡ�������ĩ�е���������Ӧ�Ļ�ѧ����ʽΪ����
��2������������Ҫ�IJ��������ǣ��ձ�����������������
��3�����ⶨ��������ֻ����CaSO4��SiO2������Ϊʵ������������ܡ����ߡ����ܡ����÷�ĩ״��ʯ��ʯ��ϡ���ᷴӦ�ƶ�����̼��
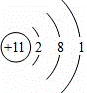
��4��Fe��Fe2��SO4��3��Ӧ�Ļ�ѧ����ʽΪ������
��5�������������ܽ��������ͼ2�����ᾧ��Ϻ��˳����壬��������ˮϴ��2��3�Σ��ñ�ˮϴ�ӵ�Ŀ���ǣ�
���ȥ������渽�ŵ����ʣ�
��������

| ���ʵ��ת�����Ʊ������˵�ԭ������������Ӧ�ã������ܽ�����������ã���Ļ�ѧ���ʣ���д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ�� | |
| ר�⣺ | ���ʵ��Ʊ��� |
| ������ | ��1����ϡ�������ĩ�е���������Ӧ��������������ˮȥ������� ��2���ӹ���ʱ���õ��������У��ձ�����������©��ȥ������� ��3���ӹ�ҵ������Ҫ�ɷ���Fe2O3��������CaCO8��SiO2���Ȳ�����ˮҲ������ϡ���ᣩ������ϡ�����Fe2O3��������CaCO3�ܹ���ϡ���ᷴӦ����Ŀ��˵�����ⶨ��������ֻ����CaSO4��SiO2��˵�������е�̼����Ѿ���ȫ��ϡ���ᷴӦ�������˶�����̼����ȥ������� ��4����ͼ��֪��Fe��Fe2��SO4��3��Ӧ����FeSO4����Ӧ����Fe��Fe2��SO4��3����������FeSO4ȥ������� ��5���������������ܽ��������ͼ1���Կ����������������ܽ�����¶ȵ����߶�����ˮ���¶ȵͣ����������ڵ����µ��ܽ��С���ɽ���ϴ�ӹ������̷����ܽ����ɵ���ʧȥ������� |
| ��� | �⣺��1��ϡ�������ĩ�е���������Ӧ��������������ˮ���䷴Ӧ�Ļ�ѧ����ʽΪ��Fe2O3+2H2SO4�TFe2��SO4��3+3H2O���ʴ�Ϊ��Fe2O3+2H2SO4�TFe2��SO4��3+3H2O�� ��2������Ŀ��ͼ���Կ��������������������Һ�壬�����Һ��������������������ǹ��ˣ�����ʱ���õ��������У��ձ�����������©�����ʴ�Ϊ��©���� ��3����ҵ������Ҫ�ɷ���Fe2O3��������CaCO8��SiO2���Ȳ�����ˮҲ������ϡ���ᣩ������ϡ�����Fe2O3��������CaCO3�ܹ���ϡ���ᷴӦ����Ŀ��˵�����ⶨ��������ֻ����CaSO4��SiO2��˵�������е�̼����Ѿ���ȫ��ϡ���ᷴӦ�������˶�����̼���壬�ʴ�Ϊ���ܣ� ��4����ͼ��֪��Fe��Fe2��SO4��3��Ӧ����FeSO4����Ӧ����Fe��Fe2��SO4��3����������FeSO4���ʷ�Ӧ�Ļ�ѧ����ʽΪ��Fe+Fe2��SO4��3�T3FeSO4�� �ʴ�Ϊ��Fe+Fe2��SO4��3�T3FeSO4�� ��5�������������ܽ��������ͼ1���Կ����������������ܽ�����¶ȵ����߶������ñ�ˮϴ�ӵ�Ŀ����һ����ȥ������渽�ŵ�����ˮ���ʣ�������ˮ���¶ȵͣ����������ڵ����µ��ܽ��С���ɽ���ϴ�ӹ������̷����ܽ����ɵ���ʧ���ʴ�Ϊ���ñ�ˮϴ�ӿɽ���ϴ�ӹ������̷�����ģ� |
| ������ | ��״��ʯ��ʯ��ϡ���ᷴӦʱ���������ɵ����������ˮ��������̼��Ƶı��棬��ֹ��̼�����ϡ����Ľ�һ���Ӵ���ʹ��Ӧֹͣ������̼��Ʒ�ĩ����������ϡ����ĽӴ������������������Ӧ���Խ��У��ʿ���̼��Ʒ�ĩ��ϡ������ȡ������̼���壮 |
��

�������ʵļ��𡢳��ӵ����������õ��Լ�������ȷ���ǣ���
| ѡ�� | ʵ��Ŀ�� | �����Լ��� |
| A | ����CO��CO2 | ͨ������ʯ��ˮ������ζ |
| B | ��������狀���� | �۲���ɫ�����ˮ |
| C | ��ȥ��ʯ��������ʯ��ʯ | ��ˮ���ϡ���� |
| D | ��ȥ����ͭ��̼�� | ��ϡ������ڿ��������� |
����ʵ�����飬����Ϊ���п���ʵ�鲻�ܳɹ����ǣ�������
| �� | A�� | �����շ�������ë�ͻ��� | B�� | �÷���ˮ����Ӳˮ����ˮ |
| �� | C�� | ��ʳ��ˮ����Ҷ����ǩ | D�� | ���ϸ����;ƾ���Һ�����ָʾ�� |
�������й��ɺ��ܽ���ȫ��ȷ��һ���ǣ�������
| A���Գ��ӵ���ʶ | B��ʳƷ��ȫ |
| ����ϡ�����ȥZn�л��е�Ag �������յķ�����ȥFe2O3�л��е�C ����̼��Ƴ�ȥCaCl2��Һ�е�HCl | ��ù��Ĵ���ϴ����������ʳ�� �����ü�ȩˮ��Һ����ˮ��Ʒ���� �۲���ά����A��ֹҹä֢ |
| C�����������ʶ | D����ѧѧ�Ƶļ�ֵ |
| �ٻ������磬˵�������ڲ����˶� �ں���ȼ�գ��д����������� �۵��ˮ���������������������Ϊ2��1 | �����Ƹ�Ч�Ͷ�ũҩ��������ʳ���� �ڿ������Ͳ��ϣ����������������� �����û�ѧ�ϳ�ҩ��������彡�� |
| �� | A�� | A | B�� | B | C�� | C | D�� | D |
����ʳ������ҪΪ�����ṩ�����ʵ��ǣ�������
| �� | A�� | ţ�� | B�� | �߲� | C�� | �� | D�� | ţ�� |
����������Һ������������Һ�������ƵĻ�ѧ���ʣ��䱾��ԭ���ǣ�������
| �� | A�� | ������ָʾ������ | B�� | ���ܽ�������������� |
| �� | C�� | ���ܽ�������������� | D�� | ��������Ԫ�غ���Ԫ�� |
���ж����������У�����ȷ���ǣ�������
| �� | A�� |
��ʧ���� | B�� |
��������� | C�� |
������ | D�� |
��ѧ�����ȶ� |
 8��2�� ��
8��2�� ��