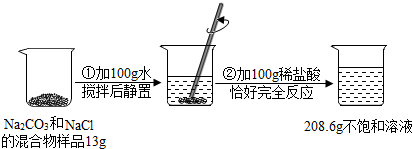
题目内容
请根据下图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题:
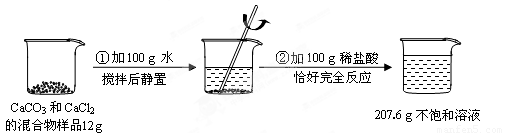
(1)实验过程中产生的CO2气体的质量为 g
(2)计算实验所用稀盐酸的溶质的质量分数(写出计算过程)。
(3)计算配制的CaCl2不饱和溶液中溶质的质量分数(写出计算过程,结果保留一位小数)。
(1)4.4
(2)7.3%
(3)6.3%
【解析】
试题分析:(1)依据质量守恒定律化学反应前后物质的总质量不变,则减少的质量为反应生成的二氧化碳的质量,即二氧化碳的质量=12g+100g+100g-207.6g=4.4g
(2) 溶质的质量分数=溶质的质量/溶液的质量 ×100% 。利用化学方程式中盐酸与二氧化碳的质量比,结合二氧化碳的质量,可求出盐酸的质量。
设盐酸中溶质的质量为x ,
CaCO3+ 2HCl == CaCl2+ H2O + CO2↑
73 44
X 4.4g
73/44 =X/4.4g X=7.3g
实验所用稀盐酸的溶质的质量分数=7.3g/100g ×100% =7.3%
(3)CaCl2不饱和溶液中溶质的质量分数=氯化钙的质量÷溶液的质量 ×100% ,生成的氯化钙的质量的质量可利用化学方程式求出,原混合物中的氯化钙可用混合物的质量减去碳酸钙的质量,碳酸钙的质量科利用化学方程式求出。
解:设原混合物中 CaCO3的质量为y ,生成的CaCl2质量为z
CaCO3+ 2HCl == CaCl2+ H2O + CO2↑
100 111 44
y z 4.4g
100/44=y/4.4g 111/44=z/4.4g
y= 10g z=11.1g
原混合物样品中CaCl2的质量为:12g-10g= 2g
配制的CaCl2不饱和溶液中溶质的质量为:2g+11.1g=13.1g
配制的CaCl2不饱和溶液中溶质的质量分数为:
13.1g÷207.6g ×100%=6.3%
答:配制的CaCl2不饱和溶液中溶质的质量分数为6.3%
考点:有关溶质质量分数的计算

 一线名师权威作业本系列答案
一线名师权威作业本系列答案