题目内容
8.请根据如图所示装置回答问题.
(1)B装置中仪器①的名称为酒精灯,收集某气体采用D装置,由此推测该气体具有的性质是该气体不与空气反应,且密度比空气小.
(2)实验室用B装置制取O2的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)若收集一瓶氧气,供做“硫粉在氧气中燃烧的实验”使用,最好选择C装置收集,理由是集气瓶底部要留少量的水.
(4)实验室制取二氧化碳选用的发生装置是A,在加试剂之前应检查装置的气密性.将纯净的二氧化碳气体通入F装置一段时间后,测得该装置中溶液的pH<(选填“>”“<”或“=”)7,因为CO2+H20=H2CO3(用化学方程式表示).
分析 (1)a为实验室常用的仪器,熟记常见仪器即可解答;根据气体的密度和溶水性确定收集装置;
(2)根据反应物的状态和反应条件确定发生装置,加热制氧气可用高锰酸钾或氯酸钾;
(3)根据二氧化硫的水溶性,集气瓶底部要留少量的水可吸收二氧化硫;
(4)实验室通常用稀盐酸与大理石反应制取二氧化碳,根据反应物的状态和反应条件确定发生装置,根据气体的密度和溶水性确定收集装置;以及二氧化碳的性质.
解答 解:(1)熟记常用仪器的名称可知a为酒精灯;根据气体的密度和溶水性确定收集装置该气体不与空气反应,且密度比空气小;
(2)高锰酸钾加热会生成锰酸钾、二氧化锰和氧气;反应物的状态是固态,反应条件是加热,应选固-固加热型的发生装置,氧气不易溶于水,可用排水法收集.故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)根据二氧化硫的水溶性,集气瓶底部要留少量的水可吸收二氧化硫;防止污染空气;故答案为:水实(4)验室通常用稀盐酸与大理石反应制取二氧化碳,反应物的状态是固态和液态,反应条件是常温,应选固-液加热型的发生装置,故选A;制取气体需要保证气密性良好,故添加药品之前要检查装置的气密性;二氧化碳和水反应生成碳酸,显酸性,所以PH<7,化学方程式为故CO2+H20=H2CO3;
故答案案为:(1)酒精灯;该气体不与空气反应,且密度比空气小;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)水;
(4)A,气密性;<;CO2+H20=H2CO3
点评 本道题比较灵活,答案也很多,要求学生要会熟练运用制取气体的发生装置和收集装置.

练习册系列答案
相关题目
3.在pH=1的无色透明的溶液中,能大量共存的是( )
| A. | K+、Ca2+、NO3- | B. | Cu2+、SO42-、NH4+ | C. | CO32-、Na+、SO42- | D. | OH-、Ba2+、C1- |
16.20℃时,将等质量的a、b两种固体,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图甲,升温到50℃时,现象如图乙,a、b两种固体的溶解度曲线如图丙.下列说法正确的是( )


| A. | 图丙中M表示b的溶解度曲线 | B. | 图甲溶液中溶质的质量分数a大于b | ||
| C. | 图乙中a可能是不饱和溶液 | D. | 30℃时a、b溶液溶质质量分数相等 |
13. 如图所示是四种元素的原子结构示意图:
如图所示是四种元素的原子结构示意图:
(1)如表是元素周期表的一部分(数字表示相应元素的原子序数),请仿照其他元素的写法将上面的A、B两种元素填入表中相应的位置(写出具体元素符号,下同):
(2)元素C的原子在化学反应中易得到(填“得到”或“失去”)电子形成离子,元素C与元素D形成化合物的化学式为MgCl2.
 如图所示是四种元素的原子结构示意图:
如图所示是四种元素的原子结构示意图:(1)如表是元素周期表的一部分(数字表示相应元素的原子序数),请仿照其他元素的写法将上面的A、B两种元素填入表中相应的位置(写出具体元素符号,下同):
| 1H | 2He | ||||||
| 3Li | 10Ne | ||||||
| 11Na | 17Cl | ||||||
17. 如图是某个化学反应的微观示意图,其中不同小球代表不同的原子,小球间的短线代表原子间的结合.从示意图中获取的信息正确的是( )
如图是某个化学反应的微观示意图,其中不同小球代表不同的原子,小球间的短线代表原子间的结合.从示意图中获取的信息正确的是( )
 如图是某个化学反应的微观示意图,其中不同小球代表不同的原子,小球间的短线代表原子间的结合.从示意图中获取的信息正确的是( )
如图是某个化学反应的微观示意图,其中不同小球代表不同的原子,小球间的短线代表原子间的结合.从示意图中获取的信息正确的是( )| A. | 图中反应前后分子没有变化 | |
| B. | 图中反应前后原子的种类与个数有变化 | |
| C. | 反应前后各元素的化合价没有变化 | |
| D. | 该反应不属于复分解反应 |
18.水是一种宝贵的自然资源.下列有关水的说法正确的是( )
| A. | 过滤能使硬水转化为软水 | |
| B. | 电解水实验说明水是由氢、氧元素组成的 | |
| C. | 活性炭能使海水转化为淡水 | |
| D. | 为防止水污染,应禁止使用化肥和农药 |
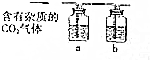 化学复习课上,某实验小组同学利用盐酸与大理石反应制取二氧化碳时,发现产生的气体经反复实验也不能使澄清石灰水变浑浊.
化学复习课上,某实验小组同学利用盐酸与大理石反应制取二氧化碳时,发现产生的气体经反复实验也不能使澄清石灰水变浑浊.