题目内容
1.“控制变量”是进行对比实验的重要手段.某同学在学完相关的化学知识后,走进实验室做了如下含有对比思想的化学实验,请你参与并回答下列问题.
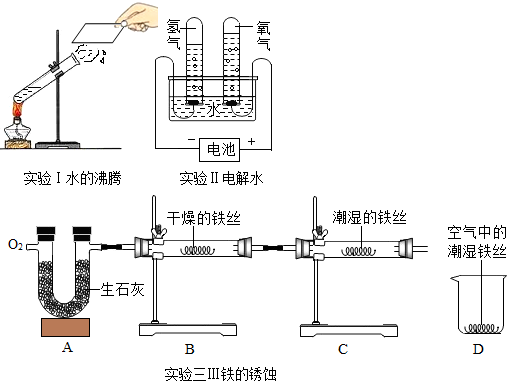
(1)根据实验Ⅰ的目的,主要对比出乒乓球碎片和滤纸碎片的着火点不同.
(2)现取实验Ⅱ现象明显后瓶①、瓶②中的液体做试样,充分加热,然后分别向其中滴加足量盐酸,观察到②(选填①或②)瓶的试样中有气泡产生,产生气泡反应的化学方程式为Na2CO3+2HCl=2NaCl+H2O+CO2↑.
(3)实验Ⅲ的烧杯B中呈现的现象能说明分子是不断运动的.当烧杯A中液体是浓氨水时烧杯B中的酚酞溶液由无色变为红色;当烧杯A中液体换成足量浓盐酸,且烧杯B中液体换成滴有少量石灰水的酚酞溶液时,一段时间后,溶液颜色的变化是由红色变成无色,此时引起溶液颜色改变反应的化学方程式为2HCl+Ca(OH)2=CaCl2+2H2O.
分析 (1)根据燃烧的条件进行解答;
(2)根据二氧化碳与氢氧化钠的反应进行分析解答;
(3)根据浓氨水、浓盐酸具有挥发性以及酸碱指示剂遇到酸碱变色情况进行解答.
解答 解:(1)实验Ⅰ的目的主要对比出乒乓球碎片和滤纸碎片的着火点不同,故填:着火点.
(2)氢氧化钠能与二氧化碳反应生成碳酸钠和水,碳酸钠能与盐酸反应生成氯化钠、水和二氧化碳,会观察到有气泡产生,故填:②,Na2CO3+2HCl=2NaCl+H2O+CO2↑.
(3)氨水呈碱性,能使酚酞试液变红;盐酸能与氢氧化钙反应生成氯化钙和水,使溶液的碱性消失,红色褪去,故填:红;由红色变成无色,2HCl+Ca(OH)2=CaCl2+2H2O.
点评 本题考查的是燃烧的条件和碱的有关性质,完成此题,可以依据已有的知识进行.

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案
相关题目
12.核电荷数为1~18的元素的原子结构示意图等信息如下,回答下列问题:
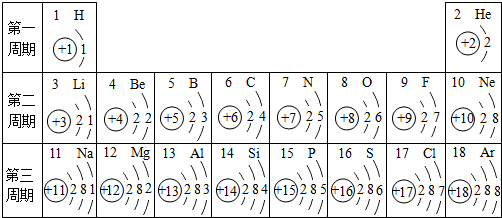
(1)在第三周期中,各原子结构的共同之处是原子核外电子层数相同;该周期中,各原子核外电子排布的变化规律是最外层电子数依次增加.
(2)在第三周期中,元素类型的变化情况是:从左到右由金属元素过渡到非金属元素,并以稀有气体结尾.
(3)写出核外电子排布与氖原子相同的阳离子和阴离子符号各一个:阳离子Na+,阴离子F-.
(4)写出含有氮元素的常见氧化物、酸、碱、盐的化学式各一个:
(5)在金属活动性顺序中镁的活动性比铝的活动性强,试从原子结构的角度说明其原因:镁铝的电子层数相同,镁原子的最外层电子数是2,铝原子的最外层电子数是3,在化学反应中镁原子更易失去电子.

(1)在第三周期中,各原子结构的共同之处是原子核外电子层数相同;该周期中,各原子核外电子排布的变化规律是最外层电子数依次增加.
(2)在第三周期中,元素类型的变化情况是:从左到右由金属元素过渡到非金属元素,并以稀有气体结尾.
(3)写出核外电子排布与氖原子相同的阳离子和阴离子符号各一个:阳离子Na+,阴离子F-.
(4)写出含有氮元素的常见氧化物、酸、碱、盐的化学式各一个:
| 物质的类别 | 氧化物 | 酸 | 碱 | 盐 |
| 物质的化学式 |
16.玉米是营养丰富的粗粮,玉米粉中的主要成分见下表.
(1)上表中含有人体所需的营养素有5类.
(2)缺钙能给人造成的影响是a(填序号,下同).
a.佝偻病及发育不良 b.贫血 c.夜盲症 d.甲状腺肿大
(3)下列物质属于最清洁的燃料是D.
A.汽油 B.用淀粉制出的乙醇 C.煤 D.氢气.
| 成分 | 蛋白质 | 糖类 | 水和维生素B等 | 钙 |
| 质量分数% | 约10 | 约80 | 约5 | 约0.23 |
(2)缺钙能给人造成的影响是a(填序号,下同).
a.佝偻病及发育不良 b.贫血 c.夜盲症 d.甲状腺肿大
(3)下列物质属于最清洁的燃料是D.
A.汽油 B.用淀粉制出的乙醇 C.煤 D.氢气.
13.下列物质属于化合物的是( )
| A. | 镁 | B. | 氧气 | C. | 蒸馏水 | D. | 金刚石 |
3.下列四个图象的变化趋势,能正确描述对应操作的是( )
| A. | 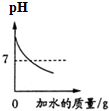 向pH=13的氢氧化钠溶液中不断加入水 | |
| B. | 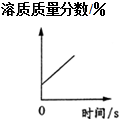 将浓盐酸敝口放置在空气中 | |
| C. |  t℃时,向饱和硝酸钾溶液中加入硝酸钾晶体 | |
| D. | 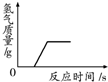 一定量的稀硫酸与锌粒反应 |