题目内容
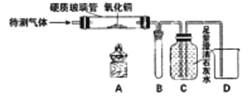
【题目】在做氧化铜,木炭反应的实验时,往往会发现充分反应后试管中仍有黑色固体。晓明对此进行了探究,并邀请你一起参与。
[提出问题]氧化铜与木炭充分反应结束后,试管中的黑色固体是什么?
[猜想假设]黑色固体可能是①木炭
②_________;③________。
[查阅资料]①铜、木炭不与稀硫酸反应。
②氧化铜能与稀硫酸反应形成蓝色溶液。
[实验验证]晓明设计的实验方案是:取少量该黑色固体在空气中灼烧,观察现象。如果猜想①正确,现象应该是______。
[实验设计]科学探究的方法有多种,请你再设计一种方法来证明晓明的猜想②或③正确。(请简明写出操作、步骤和结论)_______。
[反思整理]若试管壁上沾有了黑色固体氧化铜,除去黑色氧化铜的方法是(用化学方程式表示)________;试管洗净的标准是________。
【答案】氧化铜 氧化铜和木炭 黑色粉末减少 向盛有黑色固体的试管中加入足量的稀硫酸,充分振荡,黑色粉末消失,溶液颜色变蓝,说明猜想②正确或向盛有黑色固体的试管中加入足量的稀硫酸,充分振荡,黑色粉末减少,溶液颜色变蓝,说明猜想③正确 ![]() 管壁附着的水既不凝成水珠也不成股流下
管壁附着的水既不凝成水珠也不成股流下
【解析】
[猜想假设]
黑色固体可能是:①木炭、②未参加反应的氧化铜、③木炭和氧化铜的混合物。
[实验验证]晓明设计的实验方案是:取少量该黑色固体在空气中灼烧,观察现象。如果猜想①正确,现象应该是:黑色固体粉末减少,因为木炭燃烧产生二氧化碳气体,固体质量逐渐减少;
[实验设计]科学探究的方法有多种,设计一种方法来证明晓明的猜想②正确;
实验步骤:向盛有黑色固体的试管中加入足量的稀硫酸,充分振荡,黑色粉末完全消失,溶液颜色变蓝,因为氧化铜能与稀硫酸反应产生蓝色硫酸铜溶液;
实验结论:说明猜想②正确;
设计另一种方法来证明晓明的猜想③正确;
实验步骤:向盛有黑色固体的试管中加入足量的稀硫酸,充分振荡,黑色粉末减少,但有剩余,因为木炭不能与稀硫酸反应;溶液颜色变蓝,因为氧化铜与稀硫酸反应产生蓝色硫酸铜溶液;
实验结论:说明猜想③正确;
[反思整理]若试管壁上沾有了黑色固体氧化铜,除去黑色氧化铜的方法是:用稀硫酸与氧化铜反应产生硫酸铜溶液和水:![]() ;试管洗净的标准是:管壁附着的水既不凝成水珠也不成股流下。
;试管洗净的标准是:管壁附着的水既不凝成水珠也不成股流下。

 快捷英语周周练系列答案
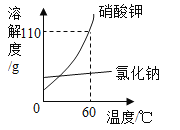
快捷英语周周练系列答案【题目】如图![]() 是甲、乙、丙三种固体物质的溶解度曲线图。
是甲、乙、丙三种固体物质的溶解度曲线图。

(1)图1中,20℃时,甲、乙、丙三种物质中,溶解度最大的是_____,50℃时,将40g乙物质放入50g水中,充分搅拌,形成溶液的质量为_____。
(2)20℃时,进行了如图![]() 所示的实验:
所示的实验:
①上述溶液中属于不饱和溶液的是_____;
②下列操作能使![]() 中溶液溶质的质量分数发生改变的是_____。
中溶液溶质的质量分数发生改变的是_____。
![]() 、加入20g乙 b、加入100g水 c、升温至40℃ d、加入150g40℃时乙的饱和溶液,再恢复至20℃
、加入20g乙 b、加入100g水 c、升温至40℃ d、加入150g40℃时乙的饱和溶液,再恢复至20℃
(3)如表是NaCI、KNO3在不同温度时的溶解度。
温度/℃ |
|
|
|
|
| |
溶解度 |
|
|
|
|
|
|
|
|
|
|
|
| |
①若要比较KNO3与NaCI在水中的溶解能力,需要控制的量是水的质量和_____。
②若将表中数据在坐标系中绘制成NaCI和KNO3的溶解度曲线,两条曲线的交点对应的温度范围是_____(填序号)。
A 0℃20℃ B 20℃40℃ C 40℃60℃ D 60℃80℃
【题目】某化学兴趣小组的同学把12g石灰石样品和100g稀盐酸(足量)放入烧杯中,在化学反应过程中对烧杯及其中剩余物进行六次称量,记录数据如下表(杂质不溶于水,也不与稀盐酸反应,烧杯的质量为25g)
反应时间(s) | t0 | t1 | t2 | t3 | t4 | t5 |
烧杯和药品质量(g) | 137 | 135 | 133.5 | 133 | 132.6 | 132.6 |
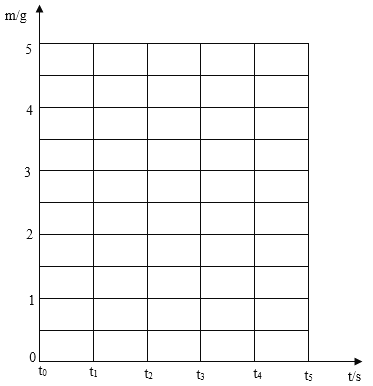
(1)反应共生成了二氧化碳 g.请计算石灰石样品中碳酸钙的质量是多少?
(2)反应完全后所得溶液中氯化钙的溶质质量分数(计算结果精确至0.1% )
(3)请在下面座标图中画出生成的气体质量(m)随时间(t)变化的曲线