题目内容
8.下列说法中正确的是( )| A. | 加入二氧化锰,过氧化氢会分解出更多氧气 | |
| B. | 蜡烛在氧气中燃烧的反应属于化合反应 | |
| C. | 空气中氧气的质量约占空气质量的$\frac{1}{5}$ | |
| D. | 人与动物的呼吸作用都属于缓慢氧化 |
分析 A、催化剂的特点可以概括为“一变二不变”,一变是能够改变化学反应速率,二不变是指质量和化学性质在化学反应前后保持不变.
B、蜡烛在氧气中燃烧生成二氧化碳和水,进行分析判断.
C、根据空气的组成成分,进行分析判断.
D、氧化反应分为剧烈氧化和缓慢氧化,根据缓慢氧化的概念进行分析解答,缓慢氧化是指反应进行的很缓慢,甚至不容易被察觉的氧化反应.
解答 解:A、催化剂只能改变化学反应速率,对生成物的质量无影响,使用催化剂不能增加生成物的质量,故选项说法错误.
B、蜡烛在氧气中燃烧生成二氧化碳和水,该反应的生成物是两种,不符合“多变一”的特征,不属于化合反应,故选项说法错误.
C、空气中氧气的质量约占空气体积(而不是质量)的$\frac{1}{5}$,故选项说法错误.
D、人与动物的呼吸作用,是与空气中的氧气发生的不容易察觉的缓慢氧化,故选项说法正确.
故选:D.
点评 本题难度不大,了解催化剂的特征、化合反应的特征、空气的组成成分、缓慢氧化的特征是正确解答本题的关键.

练习册系列答案
相关题目
18.下列说法错误的是( )
| A. | 做铁丝在氧气中燃烧的实验需要在集气瓶底留水或细砂 | |
| B. | 实验室用高锰酸钾制取氧气实验结束时,要先移开酒精灯再将导管移出水槽 | |
| C. | 用向上或向下排空气法收集气体时,导管要接近集气瓶底部 | |
| D. | 给试管里的固体加热时,要先预热,然后固定在有药品的部位加热 |
16.如图所示粒子结构示意图得出的结论中,错误的是( )


| A. | ②③④属于离子 | B. | ①②⑤属于原子 | ||
| C. | ⑤易失去电子成为阳离子 | D. | ①⑤的结构不稳定 |
13.区分下列各组物质,所用的两种方法不完全正确的一组是( )
| 选项 | 区分的物质 | 区分方法 |
| A | 黑醋和酱油 | ①闻气味 ②尝味道 |
| B | 食盐和面碱(Na2CO3) | ①加食醋 ②做馒头 |
| C | 黄金和黄铜(假黄金) | ①灼烧 ②测密度 |
| D | 蒸馏水和自来水 | ①蒸发 ②看颜色 |
| A. | A | B. | B | C. | C | D. | D |
20.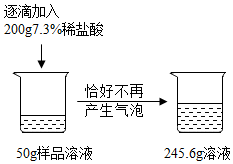 实验室有一瓶放置已久的氢氧化钠溶液,为探究其变质情况,某化学兴趣小组进行了以下探究.
实验室有一瓶放置已久的氢氧化钠溶液,为探究其变质情况,某化学兴趣小组进行了以下探究.
【猜想与假设】
猜想1:没有变质,溶质为氢氧化钠;
猜想2:部分变质,溶质为氢氧化钠和碳酸钠;
猜想3:完全变质,溶质为碳酸钠.
【实验探究1】
【实验探究2】
为了进一步确认该氢氧化钠溶液的变质情况,该小组的同学又进行了如下实验,请计算原氢氧化钠溶液中变质的氢氧化钠与未变质的氢氧化钠的质量比为1:1.
【反思与评价】
氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式CO2+2NaOH=Na2CO3+H2O,所以在实验室中必须密闭保存该物质.
 实验室有一瓶放置已久的氢氧化钠溶液,为探究其变质情况,某化学兴趣小组进行了以下探究.
实验室有一瓶放置已久的氢氧化钠溶液,为探究其变质情况,某化学兴趣小组进行了以下探究.【猜想与假设】
猜想1:没有变质,溶质为氢氧化钠;
猜想2:部分变质,溶质为氢氧化钠和碳酸钠;
猜想3:完全变质,溶质为碳酸钠.
【实验探究1】
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量该溶液与试管中,加入足量稀盐酸 | 有气泡冒出 | 氢氧化钠溶液一定变质了 |
| (2)另取少量该溶液与试管中,加入氯化钙(或CaCl2). | 有白色沉淀生成 | 猜想2正确 |
| (3)取步骤(2)试管中的少量上层清液,加入酚酞试液 | 溶液变成红色 |
为了进一步确认该氢氧化钠溶液的变质情况,该小组的同学又进行了如下实验,请计算原氢氧化钠溶液中变质的氢氧化钠与未变质的氢氧化钠的质量比为1:1.
【反思与评价】
氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式CO2+2NaOH=Na2CO3+H2O,所以在实验室中必须密闭保存该物质.
15.某种碳原子的原子核内有6个质子和6个中子,另一种碳原子核内有6个质子和8个中子,则这两种碳原子中不同的是( )
| A. | 原子的质量 | B. | 核电荷数 | C. | 核外电子数 | D. | 原子的电性 |
 某化学小组同学用如图装置制取一定量的氧气.请你参与探究:
某化学小组同学用如图装置制取一定量的氧气.请你参与探究: