题目内容
12.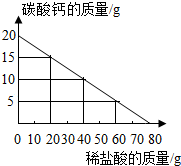 向20g碳酸钙中不断加入稀盐酸,其质量变化如图所示,请回答下列问题:
向20g碳酸钙中不断加入稀盐酸,其质量变化如图所示,请回答下列问题:(1)当20g碳酸钙恰好完全反应时,所加稀盐酸的质量为80g.
(2)所加稀盐酸的溶质质量分数为多少?(结果精确到0.01%)
分析 (1)根据图象可知:当CaCO3质量为0时,即为盐酸与CaCO3恰好完全反应的时刻,此时所用稀盐酸的量即是所消耗的稀盐酸,所以20gCaCO3完全反应时,所加稀盐酸的质量为80g;
(2)根据碳酸钙与盐酸反应的化学方程式,由碳酸钙的质量可以计算出消耗的稀盐酸的溶质质量,由溶质质量分数计算公式即可求出稀盐酸的溶质质量分数.
解答 解:(1)如图象所示:当20gCaCO3恰好完全反应时,所加稀盐酸的质量80g;
(2)设80g稀盐酸含有HCl的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73
20g x
$\frac{100}{20g}$=$\frac{73}{x}$
x=14.6g
所加稀盐酸的溶质质量分数为$\frac{14.6g}{80g}$×100%=18.25%.
故答案为:(1)80;
(2)所加稀盐酸的溶质质量分数为18.25%.
点评 根据化学方程式可以表示反应中各物质的质量关系,由其中任意一种物质的质量可计算反应中其它物质的质量.

练习册系列答案
相关题目
2.C3N4是一种新型材料,它的硬度比金刚石还大,可用作切割工具.在C3N4中C元素的化合价为+4,则N元素的化合价是( )
| A. | +4 | B. | +5 | C. | -3 | D. | +2 |
20. 化学小组把50g质量分数为98%的浓硫酸(ρ浓硫酸=1.84g/cm3)稀释为质量分数为20%的硫酸(ρ水=1g/cm3).下列叙述中正确的是( )
化学小组把50g质量分数为98%的浓硫酸(ρ浓硫酸=1.84g/cm3)稀释为质量分数为20%的硫酸(ρ水=1g/cm3).下列叙述中正确的是( )
 化学小组把50g质量分数为98%的浓硫酸(ρ浓硫酸=1.84g/cm3)稀释为质量分数为20%的硫酸(ρ水=1g/cm3).下列叙述中正确的是( )
化学小组把50g质量分数为98%的浓硫酸(ρ浓硫酸=1.84g/cm3)稀释为质量分数为20%的硫酸(ρ水=1g/cm3).下列叙述中正确的是( )| A. | 计算所需水的质量为200g | |
| B. | 按照图示步骤量取水,配置的溶液质量分数将偏小 | |
| C. | 实验室有10mL、50mL、100mL规格的量筒,量取浓硫酸应选择100mL的量筒 | |
| D. | 将浓硫酸沾到皮肤上,应立即用大量的水冲洗,再涂上3%~5%的碳酸氢钠溶液 |
17. a、b、c三种物质的溶解度曲线如图所示.下列说法正确的是( )
a、b、c三种物质的溶解度曲线如图所示.下列说法正确的是( )
 a、b、c三种物质的溶解度曲线如图所示.下列说法正确的是( )
a、b、c三种物质的溶解度曲线如图所示.下列说法正确的是( )| A. | t1℃时,a、b两种物质的溶质质量分数相同 | |
| B. | a中含有少量b时可采用降温结晶的方法提纯a | |
| C. | 将c的饱和溶液变为不饱和溶液,可采用升高温度的方法 | |
| D. | 将t2℃时a、b、c三种物质的饱和溶液降温至t1℃时,这三种溶液的溶质质量分数的大小关系是a=c>b |
1.下列物质中,能作钾肥的是( )
| A. | NH4H2PO4 | B. | NH4HCO3 | C. | CO(NH2)2 | D. | KCl |
2.根据实验要求,分析作答.
(1)如图是实验室制取气体的一组装置图,按要求回答问题:
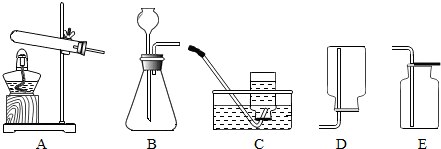
①若用装置B来制备气体,指出其中的错误:长颈漏斗下端没有伸入到锥形瓶的底部.
②H2、O2、CO2是初中常见的三种气体,实验室可选用装置B来制备的气体有H2、O2、CO2(填化学式),若制备的气体既可用装置C来收集,又可用装置D来收集,则其反应的化学方程式为Zn+H2SO4═ZnSO4+H2↑.
③实验室常用加热氯化铵和熟石灰两种固体混合物来制取氨气,化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2.则实验室制取氨气的发生装置可选用装置A(选填字母),收集氨气只能用装置D,据此氨气具有的物理性质是易溶于水且密度比空气小.
(2)某兴趣小组为了测定葡萄糖的元素组成,取一定量的葡萄糖与氧气反应,并通过测定生成CO2和H2O的质量来确定葡萄糖中元素的组成.实验装置如图,其中CuO的作用是防止反应不完全生成CO,NaOH固体、CaCl2固体、碱石灰都是常用的干燥剂.回答下列问题:
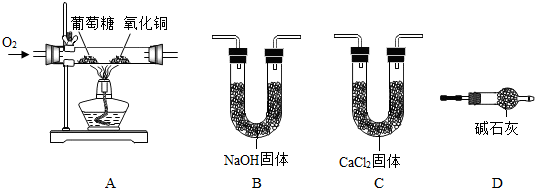
①将如图装置连接成整套实验装置,连接顺序依次为A→C→B→D(填字母).
②实验过程中数据记录如下:
反应中生成水的质量是n-mg.(用M、N或m、n表示)
③若实验不连接装置D,则测得的CO2质量偏大,原因是装置B中的氢氧化钠固体吸收了空气中的二氧化碳和水.
(1)如图是实验室制取气体的一组装置图,按要求回答问题:

①若用装置B来制备气体,指出其中的错误:长颈漏斗下端没有伸入到锥形瓶的底部.
②H2、O2、CO2是初中常见的三种气体,实验室可选用装置B来制备的气体有H2、O2、CO2(填化学式),若制备的气体既可用装置C来收集,又可用装置D来收集,则其反应的化学方程式为Zn+H2SO4═ZnSO4+H2↑.
③实验室常用加热氯化铵和熟石灰两种固体混合物来制取氨气,化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2.则实验室制取氨气的发生装置可选用装置A(选填字母),收集氨气只能用装置D,据此氨气具有的物理性质是易溶于水且密度比空气小.
(2)某兴趣小组为了测定葡萄糖的元素组成,取一定量的葡萄糖与氧气反应,并通过测定生成CO2和H2O的质量来确定葡萄糖中元素的组成.实验装置如图,其中CuO的作用是防止反应不完全生成CO,NaOH固体、CaCl2固体、碱石灰都是常用的干燥剂.回答下列问题:

①将如图装置连接成整套实验装置,连接顺序依次为A→C→B→D(填字母).
②实验过程中数据记录如下:
| 装置 | 反应前装置的质量/g | 反应后装置的质量/g |
| B | M | N |
| C | m | n |
③若实验不连接装置D,则测得的CO2质量偏大,原因是装置B中的氢氧化钠固体吸收了空气中的二氧化碳和水.
