题目内容
2.C3N4是一种新型材料,它的硬度比金刚石还大,可用作切割工具.在C3N4中C元素的化合价为+4,则N元素的化合价是( )| A. | +4 | B. | +5 | C. | -3 | D. | +2 |
分析 根据在化合物中正负化合价代数和为零,结合C3N4的化学式进行解答即可.
解答 解:C元素的化合价为+4,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+4)×3+4x=0,则x=-3价.
故选:C.
点评 本题难度不大,掌握利用化合价的原则(化合物中正负化合价代数和为零)计算指定元素的化合价的方法即可正确解答此类题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.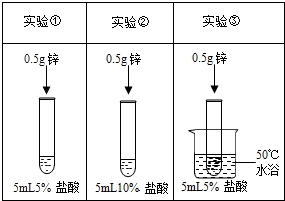 为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计了如图实验.下列说法不正确的是( )
为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计了如图实验.下列说法不正确的是( )
 为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计了如图实验.下列说法不正确的是( )
为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计了如图实验.下列说法不正确的是( )| A. | 对比实验①和②,可研究盐酸的溶质质量分数对反应剧烈程度的影响 | |
| B. | 对比实验①和③,可研究温度对反应剧烈程度的影响 | |
| C. | 对比实验②和③,可研究盐酸的溶质质量分数对反应剧烈程度的影响 | |
| D. | 此实验运用了控制变量法与对比实验法 |
7.元素周期表是学习和研究化学的重要工具.请根据如表(元素周期表的部分内容)回答有关问题:
(1)查出空气中含量最多元素的相对原子质量为14.01;
(2)在元素周期表中,同一周期中(横行)的元素,除0族(最右纵行)元素外,从左到右原子序数依次增大,原子半径逐渐减少.则原子半径:钠>镁(填“>”或“<”或“=”);
(3)第3周期第ⅥA元素的原子得到2个电子后形成了离子,该离子符号是S2-.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
| 3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(2)在元素周期表中,同一周期中(横行)的元素,除0族(最右纵行)元素外,从左到右原子序数依次增大,原子半径逐渐减少.则原子半径:钠>镁(填“>”或“<”或“=”);
(3)第3周期第ⅥA元素的原子得到2个电子后形成了离子,该离子符号是S2-.
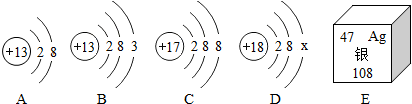
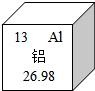 铝元素与人类关系密切. 根据如图填空:
铝元素与人类关系密切. 根据如图填空: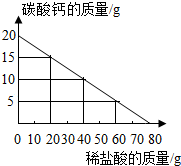 向20g碳酸钙中不断加入稀盐酸,其质量变化如图所示,请回答下列问题:
向20g碳酸钙中不断加入稀盐酸,其质量变化如图所示,请回答下列问题: