题目内容
经测定甲醛(CH2O)和乙酸乙酯(C4H8O2)组成的混合物中氧元素的质量分数为16%,则此混合物中氢元素的质量分数是( )
| A、12% | B、78% |
| C、72% | D、13% |
考点:元素的质量分数计算
专题:化学式的计算
分析:根据甲醛和乙酸乙酯的分子式可知,分子中C、H原子数之比为:1:2,二者的质量之比为:(12×1):(1×2)=6:1,其中混合物中氧元素的质量分数为16%,则C、H元素在混合物中的总质量分数为:1-16%=84%,从而可计算出混合物中氢元素的质量分数.
解答:解:甲醛的分子式为:CH2O,乙酸乙酯的分子式为:C4H8O2,二者的混合物中含有C、H、O三种元素,混合物中氧的质量分数为16%,则C、H元素在混合物中的总质量分数为:1-16%=84%,
由于甲醛和乙酸乙酯分子中C、H原子数之比为1:2,二者的质量之比为(12×1):(1×2)=6:1,
则混合物中氢元素的质量分数为84%×
=12%,
故选C.
由于甲醛和乙酸乙酯分子中C、H原子数之比为1:2,二者的质量之比为(12×1):(1×2)=6:1,
则混合物中氢元素的质量分数为84%×
| 1 |
| 6+1 |
故选C.
点评:本题考查了混合物的计算,题目难度不大,根据甲醛、乙酸乙酯的分子式组成得出C、H元素的物质的量、质量之比为解答本题的关键,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案
相关题目
单质硫是一种黄色固体,在氧气中点燃,发出蓝紫色火焰,放出大量的热,生成一种带刺激性气味的气体.判断单质硫发生化学变化的主要依据是( )
| A、生成刺激性气味的气体 |
| B、发出蓝紫色火焰 |
| C、黄色固体 |
| D、放出大量的热 |
下列物质属于氧化物的是( )
| A、生石灰(CaO) |
| B、液态氧(O2 ) |
| C、氯化钙(CaCl2) |
| D、烧碱(NaOH) |
关于H2S、H2O、H2SO4、H2四种物质的叙述中,正确的是( )
| A、都含有氢元素 |
| B、氢元素的化合价相同 |
| C、都含有1个氢分子 |
| D、都含有2个氢分子 |
2013年“世界水日”和“中国水周”活动的宣传主题为“节约保护水资源,大力建设生态文明”.下列说法正确的是( )
| A、保护水资源,禁止使用化肥、农药 |
| B、城市浇花,使用喷灌、滴灌技术 |
| C、工业废渣的任意排放,不会污染水体 |
| D、利用沉降的方法,将硬水转化成软水 |
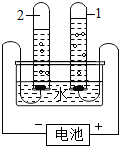 如图是电解水实验装置.
如图是电解水实验装置.