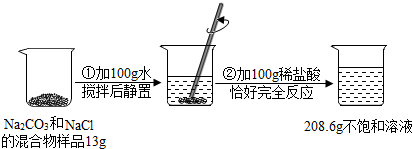
题目内容
请根据下图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题:
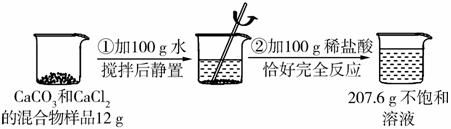
(1)实验所用稀盐酸溶质的质量分数为___________。
(2)计算原混合物样品中CaCl2的质量(写出计算过程)。
(1)7.3%
(2)解:反应中生成CO2的质量=12 g+100 g+100 g-207.6 g=4.4 g。
设原混合物中CaCO3的质量为x。
CaCO3+2HCl===CaCl2+H2O+CO2↑
100 44
x 4.4 g
 =
= 解得:x=10 g
解得:x=10 g
原混合物样品中CaCl2的质量=12 g-10 g=2 g
答:略。

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目