题目内容
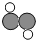
甲、乙两物质的溶解度曲线如图所示,下列叙述中正确的是( )

A. t1℃时,甲和乙的溶解度相等,都是30
B. t1℃时,将甲、乙两种物质的饱和溶液分别恒温蒸发等质量的水,析出晶体的质量一定相等
C. 温度从t2℃降至t1℃时,甲和乙的饱和溶液中析出晶体的质量甲大于乙
D. t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数
B 【解析】试题分析:A.溶解度的单位为克;B.是恒温蒸发,蒸发的水的质量相等,所以析出晶体质量也相等;C.温度从t2℃降至t1℃时,甲和乙的饱和溶液都有晶体析出,但析出晶体的质量要看原来溶液的质量,不一定是甲大于乙;D.t2℃时,甲的溶解度大于乙,但甲溶液的质量分数与乙溶液的质量分数无法比较,因为两种溶液不一定是饱和溶液甲、乙、丙有如图所示的转化关系(“→”表示反应一步实现,部分反应物和反应条件略去),下列各组物质按照甲、乙、丙的顺序排列不符合要求的是
选项 | 甲 | 乙 | 丙 |
A | C | CO2 | CO |
B | H202 | O2 | H2O |
C | CuO | Cu | Cu(N03)2 |
D | NaOH | NaCl | NaN03 |

A. A B. B C. C D. D
D 【解析】A、碳(甲)在氧气不足的情况下燃烧生成一氧化碳(乙),氧气充足的情况下生成二氧化碳(丙),一氧化碳(乙)体现可燃性或者还原性都能生成二氧化碳(丙),二氧化碳(丙)在高温下和碳反应生成一氧化碳(乙),该转化能实现,故正确;B、过氧化氢(甲)分解生成水(丙)和氧气(乙),氢气和氧气(乙)燃烧生成水(丙),水(丙)也能在通电的条件下生成氢气和氧气(乙),该转化能实现,故正确;C、氧化铜...小明在市场看到,鱼老板将一勺白色粉末加入水中,水中奄奄一息的鱼很快张开嘴,活蹦乱跳起来,小明对这种“白色粉末”很感兴趣,与小刚一起进行了相关探究。
【查阅资料】这种“白色粉末”的主要成分是过碳酸钠(化学式为Na2CO4),常温下,与水反应生成氧气.
【提出问题】过碳酸钠与水反应后得到的溶液M中溶质的成分是什么?
【作出猜想】根据质量守恒定律,Na2CO4与水反应可能生成Na2CO3、NaOH。
猜想一:Na2CO3;猜想二:NaOH;猜想三:___________。
【实验探究】
实 验 操 作 | 实 验 现 象 | 实 验 结 论 |
小刚取溶液M,滴加稀HCl | ___ | 猜想二不成立 |
小明向溶液M中滴加CaCl2溶液至不再产生沉淀为止, 用玻璃棒蘸取上层溶液,滴到pH试纸上,把试纸显示 的颜色与________比较,读出溶液的pH。 | pH=12 | ______ |
【反思拓展】
小明在实验中若选用澄清的石灰水代替CaCl2溶液,则达不到实验目的,其原因是澄清的石来水发生了如下反应_______________(用化学反应方程式表示)。
NaOH和Na2CO3 有气泡产生 标准比色卡 猜想三成立 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH(缺箭头不得分) 【解析】将一勺白色粉末加入水中,水中奄奄一息的鱼很快张开嘴,活蹦乱跳起来。【查阅资料】这种“白色粉末”的主要成分是过碳酸钠(化学式为Na2CO4),常温下,与水反应生成氧气。【提出问题】过碳酸钠与水反应后得到的溶液M中溶质的成分是什么?【作出猜想】根据质量守恒定...


 核外有18个电子,核内有16个中子,下列有关该粒子的说法中,正确的是
核外有18个电子,核内有16个中子,下列有关该粒子的说法中,正确的是
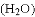 因具有许多优良特性而被科学家追捧,它是指当温度和压强达到一定值时,水的液态和气态完全交融在一起的状态,用“
因具有许多优良特性而被科学家追捧,它是指当温度和压强达到一定值时,水的液态和气态完全交融在一起的状态,用“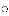
 ”表示氧原子,下列模型能表示“超临界水”分子的是
”表示氧原子,下列模型能表示“超临界水”分子的是 B.
B.  C.
C.  D.
D.