题目内容
有一食品包装说明书中注明防腐剂是苯甲酸(C6H5COOH),张华同学查资料得知苯甲酸的酸性比醋酸强,可用做食品防腐剂.下列对苯甲酸性质的推测中不合理的是( )
| A、苯甲酸溶液的pH小于7 |
| B、相同浓度的苯甲酸溶液的pH比醋酸的pH大 |
| C、苯甲酸溶液能使紫色石蕊试液变红 |
| D、苯甲酸溶液能与锌粒反应 |
考点:酸的化学性质,溶液的酸碱性与pH值的关系
专题:常见的酸 酸的通性
分析:A、苯甲酸溶液显酸性,它的pH小于7;
B、溶液中氢离子浓度越大,酸性越强,pH越小;
C、显酸性的溶液能使紫色石蕊试液变红;
D、依据酸的共性分析解答.
B、溶液中氢离子浓度越大,酸性越强,pH越小;
C、显酸性的溶液能使紫色石蕊试液变红;
D、依据酸的共性分析解答.
解答:解:A、苯甲酸溶液的pH小于7.故选项正确;
B、相同浓度的苯甲酸溶液和醋酸溶液中,苯甲酸溶液中的氢离子浓度比醋酸溶液中的氢离子浓度大,酸性强,pH小.故选项错误;
C、苯甲酸溶液能使紫色石蕊试液变红.故选项正确;
D、苯甲酸的溶液呈酸性.所以具有酸的共性,因此能与较活泼金属反应,故选项正确.
故选B.
B、相同浓度的苯甲酸溶液和醋酸溶液中,苯甲酸溶液中的氢离子浓度比醋酸溶液中的氢离子浓度大,酸性强,pH小.故选项错误;
C、苯甲酸溶液能使紫色石蕊试液变红.故选项正确;
D、苯甲酸的溶液呈酸性.所以具有酸的共性,因此能与较活泼金属反应,故选项正确.
故选B.
点评:溶液的pH大小与溶液中氢离子的浓度有关,氢离子浓度越大,酸性越强,pH越小.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
下列关于燃烧的现象的描述,正确的是( )
| A、氢气在氧气中燃烧产生大量的白烟 |
| B、铁丝在空气中剧烈燃烧,火星四射 |
| C、红磷在空气中燃烧发出耀眼的白光 |
| D、硫在氧气中燃烧会发出蓝紫色火焰 |
在一密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下存在某个反应,测得反应前后各物质的质量如下表.下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 20 | m | 20 | 20 |
| 反应后质量/g | 2 | 待测 | 32 | 26 |
| A、参加反应的甲、丙、丁的质量比为1:16:13 |
| B、乙可能是该反应的催化剂 |
| C、待测物质一定为4g |
| D、该反应是化合反应 |
下列说法正确的是( )
| A、人体缺乏维生素A会引起坏血病 |
| B、塑料保鲜膜属于有机合成材料 |
| C、食用的水产品可用甲醛水溶液侵泡、保鲜 |
| D、钾、铁、锌、碘都是人体所需的微量元素 |
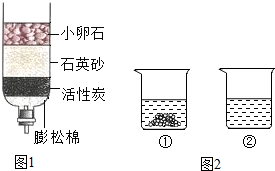 水和溶液在生活中起着十分重要的作用.
水和溶液在生活中起着十分重要的作用.