题目内容
13.生成下列图象能正确反映对应变化关系的是( )| A. |  向一定量的二氧化锰中加入过氧化氢溶液 | |
| B. |  加热一定量的高锰酸钾固体 | |
| C. |  向两份完全相同的稀盐酸中分别加入锌粉、镁粉 | |
| D. |  将水通电电解一段时间 |
分析 A、二氧化锰在过氧化氢分解的过程中充当的是催化剂,可以结合催化剂的定义来完成解答;
B、高锰酸钾分解产生了氧气,所以反应前后锰元素的质量分数要改变,可以据此解答;
C、根据氢元素的质量守恒来进行判断;
D、根据通电分解水的实验现象及结论进行解答.
解答 解:A、二氧化锰在过氧化氢分解的过程中充当的是催化剂,其质量在反应前后不会改变,故A错误;
B、高锰酸钾分解产生了氧气,使固体的总质量减少,锰元素的质量不变,所以锰元素的质量分数增加,故B错误;
C、向两份完全相同的稀盐酸中分别加入锌粉、镁粉,由于镁粉和锌粉是足量的,所以产生氢气质量应该相等,故C错误;
D、通电分解水时产生氢气的体积是氧气的二倍,故D正确.
故选D.
点评 解答这类题目时,首先,要熟记实验室制取氧气的反应原理(即实验室制取氧气的文字表达式和化学方程式),各物质的颜色、状态,反应的条件、类型,以及实验室制取氧气的反应原理和发生装置的相互联系;并且,一定要理解催化剂的概念、催化作用;等等;然后,根据所给的问题情景及相关信息,结合所学的相关知识和技能,联系起来细心地探究、推理后,按照题目要求进行选择或解答即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.前者属于物理变化,后者属于化学变化的是( )
| A. | 水结成冰,冰融化成水 | B. | 鸡蛋变臭,人体呼吸 | ||
| C. | 酒精挥发,酒精燃烧 | D. | 铁生锈,电灯通电发光 |
18.你和小明在实验室中完成二氧化碳气体的性质实验:在试管中加入2ml蒸馏水,滴入2滴石蕊试液,然后通入二氧化碳气体,观察到颜色由紫色变为红色.那么是什么物质使得石蕊试液颜色发生改变呢?
小明提出猜想:①水能使石蕊试液变色;②二氧化碳气体能使石蕊试液变色
设计实验:取用石蕊试液染成的紫色的干燥紫花分别进行如下实验.
从上面的实验可知小明的猜想都不正确,那么你的猜想是二氧化碳和水反应生成的碳酸使石蕊试液变色
实验方案现象结论及原因:
通过以上探究实验可知:往石蕊试液中通入二氧化碳气体,使石蕊试液变色的物质是碳酸.
小明提出猜想:①水能使石蕊试液变色;②二氧化碳气体能使石蕊试液变色
设计实验:取用石蕊试液染成的紫色的干燥紫花分别进行如下实验.
| 实验方案 | 现象 | 结论 | |
| 1 |  往紫花上喷水 | 紫花不变色 | 猜想①不正确 |
| 2 |  把紫花直接放入二氧化碳气体中 | 紫花不变色 | 猜想②不正确 |
| 实验方案 | 现象 | 结论及原因 |
 紫花喷水后放入二氧化碳气体中 | 紫花变红色 | 1、你的猜想正确; 2、使紫花变色的原因是(用文字表达式表示): 二氧化碳+水→碳酸 |
通过以上探究实验可知:往石蕊试液中通入二氧化碳气体,使石蕊试液变色的物质是碳酸.
3.(1)某实验小组为了探究影响金属与酸反应快慢的因素,进行如表实验:
由此得出影响金属与酸反应快慢的因素有:
如:①酸的浓度,酸的浓度越大,反应越快
②金属活动性,活动性越强,反应速率越快
③金属与酸的接触面,接触面越大,反应越快
(2)小明将一包铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到滤渣和滤液.
①锌和硝酸银溶液反应的化学方程式是Zn+2AgNO3═Zn(NO3)2+2Ag
②若滤液为蓝色,则滤液中一定含有的金属离子是Zn2+、Cu2+(写离子符号)
| 实验序号 | 实验过程 | 实验现象 |
| 1 | 镁粉和铁粉分别与5%盐酸反应 | 镁粉产生气体快 |
| 2 | 铁粉和铁片分别与15%盐酸反应 | 铁粉产生气体快 |
| 3 | 铁片分别与5%盐酸和15%盐酸反应 | 15%盐酸产生气体快 |
如:①酸的浓度,酸的浓度越大,反应越快
②金属活动性,活动性越强,反应速率越快
③金属与酸的接触面,接触面越大,反应越快
(2)小明将一包铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到滤渣和滤液.
①锌和硝酸银溶液反应的化学方程式是Zn+2AgNO3═Zn(NO3)2+2Ag
②若滤液为蓝色,则滤液中一定含有的金属离子是Zn2+、Cu2+(写离子符号)
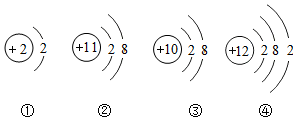 根据下列几种粒子的结构示意图,回答问题.
根据下列几种粒子的结构示意图,回答问题.