题目内容
3.某碳酸钠样品中含有少量氯化钠杂质,为测定该样品中碳酸钠的质量分数,进行了如图实验:
请回答下列问题:
(1)操作A用到的玻璃仪器除烧杯外还必需有漏斗、玻璃棒;
(2)在实验过程中加入饱和石灰水后发生反应的化学方程式是Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
(3)为探究上述反应后滤液中的溶质成分,甲同学向滤液中滴加过量稀盐酸,发现有气泡产生,则滴加盐酸前滤液中的溶质除氯化钠外还有碳酸钠、氢氧化钠.
分析 (1)过滤可除去不溶性固体物质,并根据过滤所用仪器分析解答;依据天平的使用注意事项分析解答;
(2)碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,并结合方程式的书写方法书写方程式;
(3)根据反应流程图分析滤液中有碳酸钠和氢氧化钙反应生成的氢氧化钠;滴加过量稀盐酸,发现有气泡产生,说明碳酸钠溶液过量,该滤液中还含有碳酸钠.
解答 解:(1)操作A将固体和液体分离,所以是用过滤的方法,过滤过程中用到的玻璃仪器有烧杯、漏斗、玻璃棒;
(2)样品中的氯化钠与氢氧化钙不反应,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,方程式是Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(3)滤液中有碳酸钠和氢氧化钙反应生成的氢氧化钠;另外滴加过量稀盐酸,发现有气泡产生,说明碳酸钠溶液过量,所以该滤液中还含有碳酸钠.
故答案为:(1)漏斗、玻璃棒;
(2)Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(3)碳酸钠、氢氧化钠.
点评 本题考查了学生分析和解决问题的能力,明确每一步的作用和所发生的化学反应才能正确解答.

练习册系列答案
相关题目
14.知道一些家庭防火知识和紧急灭火措施,就能避免火灾,下列说法你认为不正确的是( )
| A. | 及时更换老化破损电线,修理失灵电器 | |
| B. | 电器着火应用水扑灭 | |
| C. | 油锅中的油着火,可用锅盖盖灭 | |
| D. | 室内起火时不要急于打开门窗 |
11.检验一瓶长期暴露在空气中氢氧化钠是否变质,下列可作为检验试剂的是( )
| A. | 稀盐酸 | B. | 无色酚酞 | C. | 紫色石蕊试液 | D. | 水 |
18.下列各组内物质表示同一种物质是( )
| A. | 氢氧化钠、烧碱、火碱、苛性钠 | B. | 氢氧化钙、消石灰、生石灰 | ||
| C. | 盐酸、氯化氢、食盐 | D. | 冰、干冰、水 |
8.氢氧化钠与酸、二氧化碳反应没有明显现象.小军和小晴两位同学想用实验证明氢氧化钠能与盐酸、二氧化碳反应,他们做了以下探究过程.
【查阅资料】通常状况下,1体积水能溶解1体积二氧化碳.
【设计实验】小军设计了两个实验进行验证,请你帮他完成如表实验报告.
【反思交流】小晴认为:小军设计的上述两个实验都有缺陷,不足以证明氢氧化钠能与盐酸和二氧化碳反应.请您分析:
(1)小军的第一个实验的缺陷是用过量的盐酸,应改为适量的盐酸.
(2)小晴用上述小军第二个实验的装置和药品,验证氢氧化钠可以与二氧化碳反应,她的设计方案是:分别量取40mLNaOH和Ca(OH)2溶液放A、B中,关闭K时,B中溶液无明显变化,且通入的二氧化碳体积远大于A中溶液的体积,此实验可以说明氢氧化钠和二氧化碳发生了反应..
【实验结论】通过小晴的实验,证明了氢氧化钠可以与盐酸和二氧化碳反应.因此您认为小军的实验方案②中,装置B中无现象出现最主要的原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示)
【查阅资料】通常状况下,1体积水能溶解1体积二氧化碳.
【设计实验】小军设计了两个实验进行验证,请你帮他完成如表实验报告.
| 实验操作 | 实验现象 | 实验结论及解释 | |
| ① | 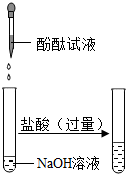 | 酚酞试液滴入氢氧化钠中变红色,滴入过量盐酸酚酞试液又变无色 | 氢氧化钠可以与盐酸反应. 该反应的化学方程式为: NaOH+HCl=NaCl+H2O |
| ② | 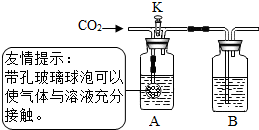 小军选用NaOH和Ca(OH)2两种溶液分别放入上边装置中的广口瓶中,关闭K,通入二氧化碳. | A、B中均无明显变化. | B中盛放的溶液是氢氧化钙. 该实验目的是 氢氧化钠可以与二氧化碳反应. |
(1)小军的第一个实验的缺陷是用过量的盐酸,应改为适量的盐酸.
(2)小晴用上述小军第二个实验的装置和药品,验证氢氧化钠可以与二氧化碳反应,她的设计方案是:分别量取40mLNaOH和Ca(OH)2溶液放A、B中,关闭K时,B中溶液无明显变化,且通入的二氧化碳体积远大于A中溶液的体积,此实验可以说明氢氧化钠和二氧化碳发生了反应..
【实验结论】通过小晴的实验,证明了氢氧化钠可以与盐酸和二氧化碳反应.因此您认为小军的实验方案②中,装置B中无现象出现最主要的原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示)
12.下列各组物质的溶液,只需用稀硫酸就能鉴别出来的是( )
| A. | NaOH、NaCl、Na2CO3 | B. | Na2CO3、Ba(NO3)2、KOH | ||
| C. | Ba(OH)2、NaNO3、KCl | D. | K2CO3、Ba(NO3)2、BaCl2 |
 化学语言包括文字语言、符号语言、图表语言等.
化学语言包括文字语言、符号语言、图表语言等.
 ,则X=11;
,则X=11;