题目内容
用化学式填写盐酸、干冰、熟石灰、蓝矾、纯碱、酒精等物质的用途。
(1)可用作改良土壤的是?????????????? ;
(2)可用作人工降雨的是????????????? ;
(3)少量存在与人体胃液中,能帮助消化的是??????????????? ;
(4)农业上用作配制波尔多液杀菌剂的是??????????????? ;
(5)各种饮用酒都含有的是?????????????? ;
(6)常用作蒸馒头、包子的发泡剂的是??????????????? 。
【答案】
(1)Ca(OH)2?? (2)CO2??? (3)HCl?? (4)Ca(OH)2??? (5)C2H5OH???? (6)Na2CO3
【解析】
试题分析:(1)熟石灰的用途①工业:制漂白粉 ,②农业:改良酸性土壤、配波尔多液? ③建筑,④涂抹在树上,既防冻又可防虫,⑤其水溶液还可以保鲜鸡蛋等,
(2)干冰升华时要吸收大量的热,从而使周围的温度降低,用于人工降雨、制冷剂等
(3)人体胃中含有少量盐酸,助消化
(4)农业上配制波尔多液杀菌剂的成分是:硫酸铜溶液和氢氧化钙的混合物
(5)各种饮用酒主要成分是:乙醇
(6)纯碱、苏打,碳酸氢钠,小苏打都能与酸反应,均可用于制作糕点所用的发酵粉
考点:常见物质的性质和用途

练习册系列答案
相关题目
 研究性学习小组对碳酸钠和碳酸氢钠的性质进行探究,请你参与实验.
研究性学习小组对碳酸钠和碳酸氢钠的性质进行探究,请你参与实验.
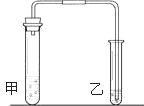
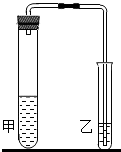
(1)我们在学习碳酸钠和碳酸氢钠的时候,做过如如图装置的实验.向盛有0.5g碳酸钠的试管里加入2mL盐酸,迅速用带导管的胶塞塞紧试管口,并将导管另一端通入盛有澄清石灰水的试管中,观察现象.用碳酸氢钠代替碳酸钠进行上述实验,观察现象.
通过比较试管甲中的两次反应,填写下表:
| 碳酸钠+盐酸 | 碳酸氢钠+盐酸 | |
| 实验现象 | ||
| 化学反应方程式 |
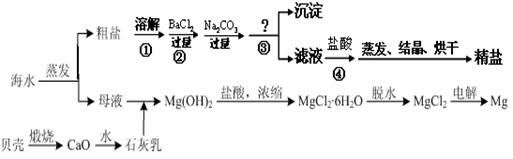
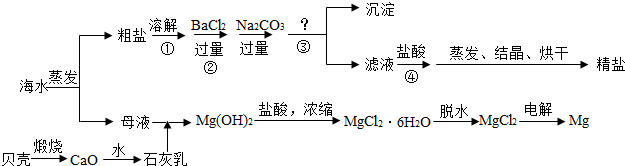
(2)以前实验室制备纯碱(Na2CO3)的主要步骤为:将饱和NaCl溶液倒入烧杯加热,控制30-35℃,搅拌下分批加入研细的NH4HCO3固体,加料完毕,保温30分钟,静置、过滤得NaHCO3晶体.用少量蒸馏水洗涤除去杂质、抽干,转入蒸发皿中灼烧得Na2CO3固体.
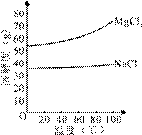
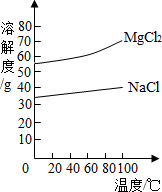
四种盐在不同温度下的溶解度表:(g/100g水)
温度 溶解度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | - | - | - | - |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
②过滤所得母液中含有NaHCO3、NaCl、NH4Cl、NH4HCO3,加入适当试剂并作进一步处理,使______(填化学式)循环使用,回收得到NH4Cl晶体.
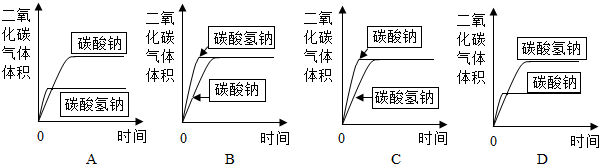
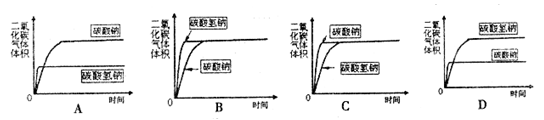
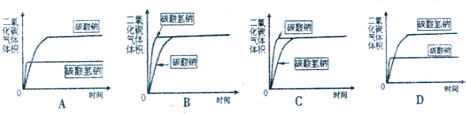
(3)分别取碳酸氢钠4.2g和碳酸钠5.3g放入相同大小的锥形瓶中,分别在密闭条件下加入相同质量、相同浓度的盐酸(足量).在相同的条件下,测量出生成气体的体积,得到时间-体积关系曲线图应为______.
通过分析和计算说明你的理由.
 (2012?鼓楼区一模)研究性学习小组对碳酸钠和碳酸氢钠的性质进行探究,请你参与实验.
(2012?鼓楼区一模)研究性学习小组对碳酸钠和碳酸氢钠的性质进行探究,请你参与实验.