题目内容
除去下列混合物中的杂质在横线上填写所选的试剂,(4、5、6、填分离方法)
①HNO3(HCl) ②NaOH(Ca(OH)2) ③NaNO3(Na2SO4)
④碳酸钙(碳酸钠) ⑤NaCl (CaCO3)固体 ⑥生石灰(碳酸钙)
⑦铜粉(氧化铜) ⑧CO2(CO) ⑨CO(CO2) .
①HNO3(HCl)
④碳酸钙(碳酸钠)
⑦铜粉(氧化铜)
考点:物质除杂或净化的探究,常见气体的检验与除杂方法,酸的化学性质,碱的化学性质,盐的化学性质
专题:物质的分离、除杂、提纯与共存问题
分析:根据除杂质至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质,以此来解答.
根据混合物的性质的不同,如沸点、溶解性以及其它化学性质进行除杂.
根据混合物的性质的不同,如沸点、溶解性以及其它化学性质进行除杂.
解答:解:①加入适量AgNO3溶液.HNO3与AgNO3溶液不反应,HCl与AgNO3溶液反应生成AgCl沉淀和HNO3溶液,从而除去杂质HCl;
故填:AgNO3溶液;
②加入适量Na2CO3溶液.碳酸根离子与钙离子结合生成碳酸钙沉淀,从而除去杂质.
故填:Na2CO3溶液;
③加入适量Ba(NO3)2溶液.硫酸根离子与钡离子结合生成硫酸钡沉淀,从而除去杂质.
故填:Ba(NO3)2溶液;
④碳酸钙不溶于水,碳酸钠溶于水,所以可以采取过滤的方法除去碳酸钠.
故填:溶解、过滤;
⑤过滤、蒸发、结晶.NaCl固体易溶于水,CaCO3固体不溶于水,所以通过过滤除去CaCO3固体,然后通过蒸发、结晶得到NaCl固体;
故填:过滤、蒸发、结晶;
⑥加热法.碳酸钙在高温下分解生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质.
故填:加热法;
⑦加入足量稀盐酸.铜与盐酸不反应,氧化铜与盐酸反应,加入足量的盐酸,充分反应后过虑即可;
故填:稀盐酸;
⑧将气体通过灼热的氧化铜.根据一氧化碳可与灼热的氧化铜反应,可将混合气体通过灼热的氧化铜从而将一氧化碳除去;
故填:灼热的氧化铜;
⑨将气体通过氢氧化钠溶液或足量的澄清石灰水(合理均可).根据二氧化碳可与氢氧化钠溶液、氢氧化钙溶液反应,并可与炽热的炭反应,可将混合气体通过氢氧化钠溶液或或足量的澄清石灰水,操作简便;
故填:氢氧化钠溶液或足量的澄清石灰水(合理均可).
故填:AgNO3溶液;
②加入适量Na2CO3溶液.碳酸根离子与钙离子结合生成碳酸钙沉淀,从而除去杂质.
故填:Na2CO3溶液;
③加入适量Ba(NO3)2溶液.硫酸根离子与钡离子结合生成硫酸钡沉淀,从而除去杂质.
故填:Ba(NO3)2溶液;
④碳酸钙不溶于水,碳酸钠溶于水,所以可以采取过滤的方法除去碳酸钠.
故填:溶解、过滤;
⑤过滤、蒸发、结晶.NaCl固体易溶于水,CaCO3固体不溶于水,所以通过过滤除去CaCO3固体,然后通过蒸发、结晶得到NaCl固体;
故填:过滤、蒸发、结晶;
⑥加热法.碳酸钙在高温下分解生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质.
故填:加热法;
⑦加入足量稀盐酸.铜与盐酸不反应,氧化铜与盐酸反应,加入足量的盐酸,充分反应后过虑即可;
故填:稀盐酸;
⑧将气体通过灼热的氧化铜.根据一氧化碳可与灼热的氧化铜反应,可将混合气体通过灼热的氧化铜从而将一氧化碳除去;
故填:灼热的氧化铜;
⑨将气体通过氢氧化钠溶液或足量的澄清石灰水(合理均可).根据二氧化碳可与氢氧化钠溶液、氢氧化钙溶液反应,并可与炽热的炭反应,可将混合气体通过氢氧化钠溶液或或足量的澄清石灰水,操作简便;
故填:氢氧化钠溶液或足量的澄清石灰水(合理均可).
点评:本题考查混合物的分离、提纯,明确除杂的原则及物质的性质、分离提纯的方法是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
下列做法中,不会对人体造成伤害的是( )
| A、做馒头是加入适量的纯碱使馒头松软 |
| B、用工业酒精配制各种酒类 |
| C、用氢氧化钠治疗胃酸过多 |
| D、用少量工业用盐烹调食物 |
如图所示装置中,若由a处进气,则可以用此装置收集的一组气体是( )


| A、O2、CH4 |
| B、CO2、CH4 |
| C、CH4、H2 |
| D、O2、CO2 |
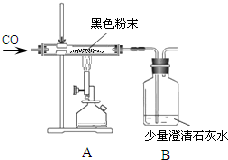 小新同学为确定某份黑色粉末,称取该粉末8.0g装入硬质玻璃管中,按如图在通风橱中进行实验.开始时缓缓通入CO气体,过一段时间后再加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关装置和物质的总质量,其数据如下表:
小新同学为确定某份黑色粉末,称取该粉末8.0g装入硬质玻璃管中,按如图在通风橱中进行实验.开始时缓缓通入CO气体,过一段时间后再加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关装置和物质的总质量,其数据如下表: