题目内容
19. 某合金的主要成分有锌、铜、碳等物质,为测定合金的某些含量做如下实验:
某合金的主要成分有锌、铜、碳等物质,为测定合金的某些含量做如下实验:(1)配制溶质质量分数为10%的稀硫酸
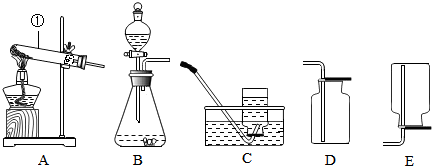
①配制200g溶质质量分数为10%的稀硫酸.需图1所示的浓硫酸的质量20.4g
②稀释浓硫酸酸时-定要A(填A或B)
A.将浓硫酸沿着烧杯内壁缓缓倒入水中
B.将水沿着烧杯内壁缓缓倒入浓硫酸中
③因为浓硫酸具有吸水性,所以常用作干燥剂.
(2)取10g合金样品放入烧杯中,向其中加入(1)中配制好的稀硫酸,产生气体的质量与加入稀硫酸的质量关系如图2所示(合金中只有锌能与稀硫酸反应)计算该合金样品中锌的质量.
分析 (1)①根据溶液稀释前后溶质质量不变进行分析;
②根据稀释浓硫酸时,一定要将浓硫酸慢慢滴入水中进行分析;
③根据浓硫酸有吸水性进行分析;
(2)根据化学方程式和题中的数据进行计算.
解答 解:(1)①需浓硫酸的质量为:$\frac{200g×10%}{98%}$=20.4g;
②稀释浓硫酸时,一定要将浓硫酸慢慢滴入水中,故选:A;
③因为浓硫酸具有吸水性,所以常用作干燥剂;
(2)设参加反应的锌的质量为x
Zn+H2SO4=ZnSO4+H2↑
65 98
x 10%×98g
$\frac{65}{x}$=$\frac{98}{10%×98g}$
x=6.5g
故答案为:(1)20.4g,A,吸水性;
(2)6.5g.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
7.下列不能用质量守恒定律解释的现象是( )
| A. | 蜡烛燃烧后质量减少 | B. | 铁丝生锈后质量增加 | ||
| C. | 潮湿的衣服在阳光下晒干 | D. | 高锰酸钾加热后固体质量减少 |
1.人们在工作、生活中,为防止事故发生常采用一些安全措施,下列安全措施中正确的是( )
| A. | 被围困在火灾区时,用湿毛巾捂住口鼻低下身子逃生 | |
| B. | 冬天用煤取暖时封闭门窗 | |
| C. | 到煤窑中挖煤用火把照明 | |
| D. | 厨房内煤气泄漏打开排气扇通风 |
18.写出除去下列各物质中的杂质所用的试剂及相应的化学方程式(括号内为杂质)
| 混合物 | 所用试剂 | 化学方程式 |
| FeSO4溶液(CuSO4) | 铁粉 | Fe+CuSO4═FeSO4+Cu |
| NaCl(Na2CO3) | 稀盐酸 | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |