题目内容
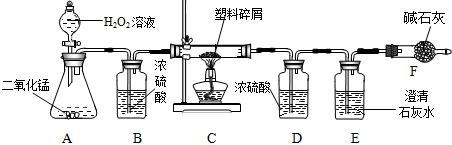
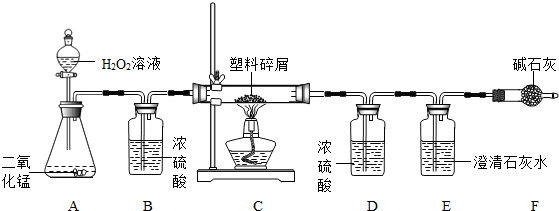
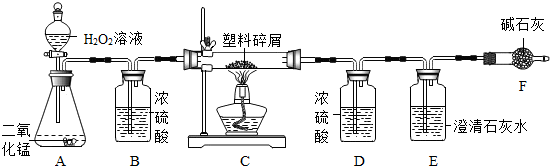
由于大量使用一次性塑料方便袋而造成的“白色污染”已成为一个严重的社会问题。某化学研究小组的同学对某种塑料袋的组成进行分析研究(资料显示该塑料只含C、H两种元素)。他们设计了图18所示的实验装置,使该塑料试样在纯氧中完全燃烧,观察实验现象、分析有关数据、推算元素含量。

(1)实验装置中有一处明显错误,请指出错误处,并写出(或在答题卷上画出正确图并用字母标注上哪一个装置)改正方法
(2) 装置F的作用是 .
(3) 若装置C的玻璃管中放入的塑料试样质量为5.9g,塑料试样充分燃烧后,装置D增重7.2g,则该塑料试样中含氢元素的质量为 g;假设塑料的组成为CxHy,则装置C的玻璃管中反应的化学方程式为 (化学计量数用含x、y的代数式表示,且可以是分数)
(4)若装置中没有连接装置B,将使该塑料试样中氢元素的质量测算结果 ( 填“偏小”、“ 偏大”或“无影响” )
【答案】
(1) B B中左边的导管应伸入液面下,右边的导管稍伸进瓶塞不能伸入液面下
(2) 防止空气中CO2对实验的干扰

(3) 0.8 , CxHy+ (4x+y)/4O2=xCO2 +y/2H2O(其它合理答案也可)
(4) 偏大
【解析】B中左边的导管应伸入液面下,右边的导管稍伸进瓶塞不能伸入液面下
要想测定塑料组成中的各元素的含量,需要除去其他干扰成分,使用碱石灰能将空气中的水蒸气和二氧化碳除掉,
该塑料试样中氢元素的质量为:7.2g× ×100%=0.8g
×100%=0.8g
若装置中没有连接仪器B,反应生成的氧气中的水蒸气进入D中被浓硫酸吸收,使得水的质量比反应生成的水的质量偏大,通过计算使得氢元素的质量偏大.

练习册系列答案
相关题目