题目内容
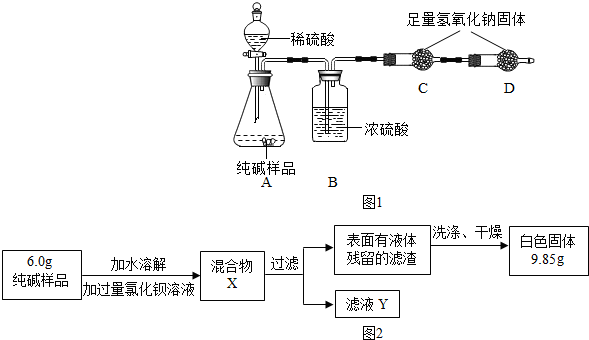
9.如图,这四位同学描述的是同一化学符号,此化学符号是( )
| A. | H2SO4 | B. | O3 | C. | SO2 | D. | NH3 |
分析 根据化学式的意义进行分析:①宏观意义:a.表示一种物质; b.表示该物质的元素组成; ②微观意义:a.表示该物质的一个分子; b.表示该物质的分子构成;据此进行分析判断.
解答 解:根据题意,该物质由两种元素组成,1个分子由3个原子构成.
A、H2SO4是由三种元素组成的,故选项不符合题意.
B、O3是由同种元素组成的,故选项不符合题意.
C、SO2由两种元素组成的,且1个分子由3个原子构成,故选项符合题意.
D、NH3是由两种元素组成的,但1个分子由4个原子构成,故选项不符合题意.
故选:C.
点评 本题难度不大,考查化学式的意义,由图示确定该物质由两种元素组成、1个分子由3个原子构成是正确解答本题的关键.

练习册系列答案
相关题目
19.下列实验操作正确的是( )
| A. | 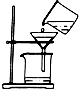 过滤 | B. | 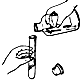 液体的倾倒 | C. |  闻气体气味 | D. | 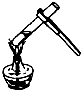 加热液体 |
20.归纳与总结是学好化学的重要方法.下列对所学知识的整理,存在错误的是( )
| A. | 分离或制取物质与原理的对应关系 ①分离液态空气制取氧气、氮气等-物质沸点不同 ②可利用氯酸钾或高锰酸钾制取氧气的原因之一-物质中含有氧元素 | |
| B. | 燃烧事实与促进燃烧方法的对应关系 ①化油器将汽油喷成雾状,进入内燃机汽缸-增大可燃物与氧气的接触面积 ②用煤炭烧锅炉时,要用鼓风机不断吹入空气-增大氧气的浓度 | |
| C. | 化学概念与逻辑关系的对应 ①氧化反应与化合反应-交叉关系 ②单质与化合物-并列关系 | |
| D. | 物质性质与用途的对应关系 ①二氧化碳本身不燃烧也不支持燃烧-用于灭火 ②稀有气体几乎不与任何物质发生化学反应-用于制造霓虹灯 |
4.为确保生命安全,下列处理事故的方法不正确的是( )
| A. | 桌面上酒精灯内酒精洒出,着火燃烧,立即用湿抹布扑灭 | |
| B. | 厨房内管道煤气(主要成分是CO)泄漏,立即关闭阀门并开窗通风 | |
| C. | 进入深洞,燃着的火把熄灭立即停止前进,退出山洞 | |
| D. | 炒菜时油锅着火,立刻浇水灭火 |
14.工业上制取ClO2的反应为:Cl2+2NaClO2═2X+2ClO2,则X的化学式为( )
| A. | NaClO | B. | NaCl | C. | NaCl2 | D. | Na |
19.下列各组物质在水溶液中能够共存,而且加入酚酞显红色的是( )
| A. | NaOH、CuSO4、H2SO4 | B. | NaCl、Ba(NO3)2、HCl | ||
| C. | NaCl、Na2SO4、Na2CO3 | D. | NH4NO3、NaOH、NaCl |