题目内容
3.请根据如图实验装置,回答下列问题: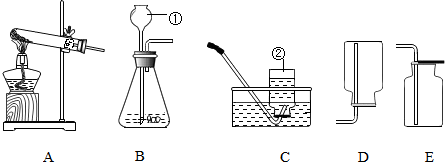
(1)写出有标号的仪器名称:①是长颈漏斗,②是集气瓶.
(2)实验室用高锰酸钾制取氧气的化学方程式为2KMnO$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,制取氧气的装置组合为AC或AE.
(3)实验室制取二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,发生装置为B.
(4)氨气(NH3)是一种密度比空气小且极易溶于水的气体,氨气的水溶液能使酚酞试液变红,在实验室用加热氯化铵和氢氧化钙的固体混合物来制取氨气,则制取氨气的发生装置是A;收集装置是D,检验是否集满的方法是用湿润的红色石蕊试纸靠近试管口,如果试纸变蓝,则证明是已经集满.
分析 (1)根据实验室常用仪器解答;
(2)根据反应物状态和反应条件选择发生装置,据气体的密度和溶解性选择收集装置,据反应原理书写方程式,;
(3)实验室制取二氧化碳气体,用大理石和稀盐酸常温反应制取,不需加热,属于固液常温型解答;
(4)实验室用氯化铵和氢氧化钙在加热条件下制备氨气,利用固体+固体加热制备气体选择气体发生装置,根据氨气是易溶于水的比空气轻的气体选择收集装置;根据氨气的水溶液显碱性解答.
解答 解:
(1)据实验室常用仪器可知:①长颈漏斗;②集气瓶;
(2)实验室可用加热高锰酸钾的方法制取氧气,属于固固常温型,选A,氧气的密度比空气大且不易溶于水,所以可用向上排空气法或排水法收集,利用高锰酸钾制取氧气方程式是:2KMnO$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)实验室制取二氧化碳气体,用大理石和稀盐酸常温反应制取,不需加热,属于固液常温型,选择发生装置B,二氧化碳密度比空气大且能溶于水,所以用向上排空气法收集,反应方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(4)实验室用氯化铵和氢氧化钙在加热条件下制备氨气,利用固体+固体加热制备气体选择气体发生装置为A,氨气是易溶于水的比空气轻的气体,需要用向下排空气方法收集氨气,所以选择装置E;根据氨气的水溶液显碱性,检验是否集满的方法是:用湿润的红色石蕊试纸靠近试管口,如果试纸变蓝,则证明是已经集满;
故答案为:
(1)①长颈漏斗;②集气瓶
(2)2KMnO$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ AC或AE
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑ B
(4)A,D; 用湿润的红色石蕊试纸靠近试管口,如果试纸变蓝,则证明是已经集满;
点评 本题考查氨的实验探究,题目难度中等,注意实验室制备氨气的所用药品,氨气的检验方法.了解发生装置和收集装置的选择依据,及反应原理,并能正确书写方程式是解答问题的关键.

| A. | 镁带在氧气中燃烧:Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2(化合反应) | |
| B. | 比较铜、银两种金属的活动性:Cu+2AgNO3=Cu(NO3)2+2Ag(置换反应) | |
| C. | 用过氧化氢溶液制取氧气:H2O2$\frac{\underline{\;MnO_2\;}}{\;}$H2O+O2↑(分解反应) | |
| D. | 用氢氧化铝治疗胃酸过多:Al(OH)3+2HCl=AlCl2+2H2O(复分解反应) |
| A. | 使空气产生雾霾的原因之一,是某些农民在秋收后或春耕前大量焚烧秸秆带来的烟尘 | |
| B. | 空气中含有大量二氧化碳气体,能产生pH=6的酸雨 | |
| C. | 空气中含量最多的氮气,在电闪雷鸣时能“雷雨发庄家”时做氮肥 | |
| D. | 空气中的氧气,来自植物的光合作用.所以保护空气就多养花、多植树造林 |
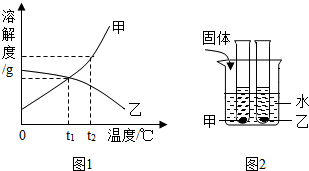
| A. | t2℃时,甲、乙两种物质的饱和溶液中溶质的质量分数大小关系为:甲>乙 | |
| B. | 将甲、乙两种物质的饱和溶液都从t2℃降至t1℃时,两种溶液中溶质的质量分数相等 | |
| C. | 向烧杯的水中加NH4NO3固体后,只有盛放甲溶液的试管中有晶体析出 | |
| D. | 向烧杯的水中加NaOH固体后,只有乙溶液中溶质的质量分数变小 |
| A. | 人体缺少碘元素会导致骨质疏松 | |
| B. | 铁生锈是铁与氧气、水共同作用的结果 | |
| C. | 空气中二氧化碳浓度越大其毒性越强 | |
| D. | 木材着火用水浇灭是降低了木材的着火点 |
| A. | 元素种类 | B. | 分子间的间隔 | C. | 分子的种类 | D. | 分子的总数 |

| A. | 该实验说明一氧化碳具有还原性 | |
| B. | 该实验说明生成物二氧化碳的密度比空气大 | |
| C. | 该实验说明一氧化碳和氧化铜的反应需要加热 | |
| D. | 该实验可以防止有毒的一氧化碳气体对空气的污染,同时又可以充分利用能源 |
| 物质 | X | O2 | CO2 | H2O |
| 反应前质量/g | 23 | 70 | 1 | 0 |
| 反应后质量/g | 0 | 待测 | 45 | 27 |
| A. | 该反应属于氧化反应 | B. | 反应中X和水的质量比为23:27 | ||
| C. | 表中待测的值为22 | D. | X中不含氧元素 |
 酸、碱、盐的化学性质是初中化学的核心知识.如图A-E是初中化学常见的酸、碱、盐,其中A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为不溶于硝酸白色沉淀.:“→”表示一种物质能转化为另一种物质(部分反应物、生成物及反应条件已省略).
酸、碱、盐的化学性质是初中化学的核心知识.如图A-E是初中化学常见的酸、碱、盐,其中A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为不溶于硝酸白色沉淀.:“→”表示一种物质能转化为另一种物质(部分反应物、生成物及反应条件已省略).