题目内容
11.甲、乙两种固体物质的溶解曲线如图t2℃时,分别盛甲、乙两种物质饱和溶液的试管放在装有同温度水的烧杯中,如图2.不考虑溶剂的蒸发.根据图象和有关信息判断,下列说法中错误的是( )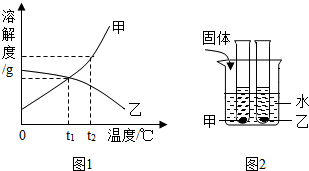
| A. | t2℃时,甲、乙两种物质的饱和溶液中溶质的质量分数大小关系为:甲>乙 | |
| B. | 将甲、乙两种物质的饱和溶液都从t2℃降至t1℃时,两种溶液中溶质的质量分数相等 | |
| C. | 向烧杯的水中加NH4NO3固体后,只有盛放甲溶液的试管中有晶体析出 | |
| D. | 向烧杯的水中加NaOH固体后,只有乙溶液中溶质的质量分数变小 |
分析 A、饱和溶液溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%;
B、根据物质的溶解度曲线可以判断随着温度的变化,溶质质量分数变化的情况;
C、硝酸铵溶于水后吸收热量,能使溶液温度降低;
D、氢氧化钠固体溶于水后放出热量,能使溶液温度升高.
解答 解:A、t2℃时,甲的溶解度大于乙的溶解度,甲、乙两种物质的饱和溶液中溶质的质量分数大小关系为甲>乙,该选项说法正确;
B、由于甲在t1℃时的溶解度大于乙在t2℃时的溶解度,将甲、乙两种物质的饱和溶液都从t2℃降至t1℃时,甲的溶质质量分数大于乙的溶质质量分数,该选项说法不正确;
C、向烧杯的水中加NH4NO3固体后,溶液温度降低,乙变成不饱和溶液,没有晶体析出,只有盛放甲溶液的试管中有晶体析出,该选项说法正确;
D、向烧杯的水中加NaOH固体后,溶液温度升高,甲变成不饱和溶液,溶质质量分数不变,乙由晶体析出,溶质质量分数减小,该选项说法正确.
故选:B.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
相关题目
2.下列各组物质在溶液中能大量共存,且形成无色溶液的是( )
| A. | H2SO4 Na2SO4 KNO3 | B. | FeCl2 H2SO4 NaNO3 | ||
| C. | Ba(OH)2 CaCl2 HCl | D. | HNO3 K2CO3 NaCl |
6.下列化学式与指定物质的主要成分或俗名对应正确的是( )
| A. | Ca(OH)2--生石灰 | B. | C2H5OH--液化石油气 | ||
| C. | NaOH--烧碱 | D. | Na2CO3--小苏打 |
16.下列说法正确的是( )
| A. | 电解水时,负极产生的气体能支持燃烧 | |
| B. | 洗洁精能将油污溶解掉,它是常用的餐洗剂 | |
| C. | 能导电的溶液中存在自由移动的离子 | |
| D. | pH小于7的降水都属于酸雨 |
 天然苏打水含有天然的碳酸氢钠及多种适应人体需求的微量元素,是一种健康饮品.根据图“XX天然苏打水”商标上的部分文字用化学用语填空:
天然苏打水含有天然的碳酸氢钠及多种适应人体需求的微量元素,是一种健康饮品.根据图“XX天然苏打水”商标上的部分文字用化学用语填空: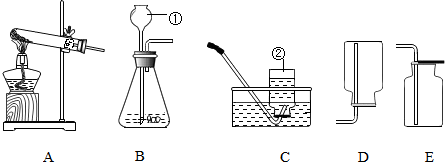
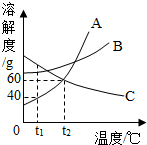 如图是A、B、C三种物质的溶解度曲线,请回答:
如图是A、B、C三种物质的溶解度曲线,请回答: 在2015年3月两会的《政府工作报告》中.李克强总理在谈到环保时,十分敏锐地指出:“环境污染是民生之患、民心之痛.要铁腕治理'
在2015年3月两会的《政府工作报告》中.李克强总理在谈到环保时,十分敏锐地指出:“环境污染是民生之患、民心之痛.要铁腕治理'