题目内容
5. (1)生活中人们常说:①高原上缺氧 ②海产品中含锌 ③胃酸过多 ④硬水中含较多钙、镁离子.请用化学用语表示:
(1)生活中人们常说:①高原上缺氧 ②海产品中含锌 ③胃酸过多 ④硬水中含较多钙、镁离子.请用化学用语表示:①中的“氧”O2;②中的“锌”Zn;③中的“酸”HCl;④中的“镁离子”Mg2+
(2)完成下列变化的化学方程式,并按要求填空.
①电解水:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,正极上与负极上产生气体体积比为1:2;
②铝制品不易被氧化,原因是:4Al+3O2═2Al2O3 用符号表示生成物中铝的化合价是$\stackrel{+3}{A{l}_{2}}{O}_{3}$;
③植物的光合作用:6CO2+6H2O$\frac{\underline{\;\;\;光照\;\;\;}}{叶绿素}$6C6H12O6+6CO2,生成的有机物中碳元素的质量分数是40%;
④用赤铁矿来炼铁:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,使用CO前必须要验纯.
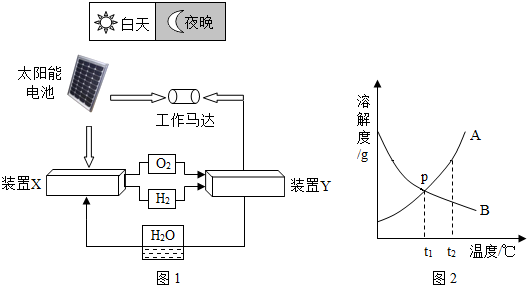
(3)如图是A、B两种固体物质的溶解度曲线.回答:
①在40℃时,等质量的A、B物质的饱和溶液降温到30℃时溶液质量的关系A小于B(选填“大于”、“小于”或“等于”);
②30℃时,130gA的饱和溶液,升温到40℃时,至少需加入A物质的质量为20g才能变成饱和溶液.
③当A中混有少量B时,用降温结晶或冷却热饱和溶液方法可以提纯固体A.
分析 (1)①高原上缺氧,氧指氧气;书写化学式即可;
②海产品中含锌,指锌元素;依据元素符号的书写方法解答;
③胃酸过多,胃酸指盐酸;依据化合物的书写方法解答;
④硬水中含镁离子.根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字;进行解答.
(2)①根据电解水生成氢气和氧气解答;
②根据铝制品不易被氧化,原因是铝和氧气反应生成一层致密的氧化膜解答;
③根据植物的光合作用的原理解答;
④根据高温条件下一氧化碳与氧化铁反应生成铁和二氧化碳解答;
(3)①据AB的溶解度随温度的降低的变化情况分析降温后溶液的质量变化;
②据该温度下A的溶解度判断所加物质能否全部溶解,从而判断溶液的质量及是否是饱和溶液;
③据AB的溶解度受温度影响情况分析提纯A的方法;
解答 解:(1)①高原上缺氧,氧指氧气;表示为:O2;故答案为:O2;
②海产品中含锌,指锌元素;元素符号表示为:Zn;故答案为:Zn;
③胃酸过多,胃酸指盐酸;依据化合物的书写方法表示为:HCl;故答案为:HCl;
④硬水中含镁离子.根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字;
所以镁离子表示为:Mg2+;故答案为:Mg2+.
(2)①电解水生成氢气和氧气,化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,正极上与负极上产生气体体积比为1:2,
②铝制品不易被氧化,原因是铝和氧气反应生成一层致密的氧化膜,化学方程式为:4Al+3O2═2Al2O3 氧化铝中铝的化合价是:$\stackrel{+3}{A{l}_{2}}{O}_{3}$
③植物的光合作用的原理是:6CO2+6H2O $\frac{\underline{\;\;\;光照\;\;\;}}{叶绿素}$ 6C6H12O6+6CO2,生成的有机物中碳元素的质量分数是$\frac{12×6}{12×6+1×12+16×6}×$100%=40%:
④高温条件下一氧化碳与氧化铁反应生成铁和二氧化碳,故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;使用CO前必须要验纯;
(3)①A的溶解度随温度的升高而增大,且变化较大,B的溶解度随温度的升高而减小,所以将40℃时等质量的A、B物质的饱和溶液降温到30℃时,A析出晶体,B变为不饱和溶液,溶液质量不变,故降温后A溶液的质量小于B;
②30℃时,A的溶解度是30g,130gA的饱和溶液有溶质30g,40℃时,A的溶解度是50g,升温到40℃时,至少需加入A物质的质量,50g-30g=20g;
③A的溶解度随温度的升高而增大,且变化较大,B的溶解度随温度的升高而减小,所以若A中混有少量B,可采用先在较高温度下配成饱和溶液,然后降温过滤,即降温结晶或冷却热饱和溶液的方法;
答案:
(1)①O2 ②Zn ③HCl ④Mg2+
+3
(2)①2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,1:2
②4Al+3O2═2Al2O3 $\stackrel{+3}{A{l}_{2}}{O}_{3}$
③6CO2+6H2O $\frac{\underline{\;\;\;光照\;\;\;}}{叶绿素}$ 6C6H12O6+6CO2 40%
④Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 验纯
(3)①小于 ②20 ③降温结晶或冷却热饱和溶液
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础.

 全能测控期末小状元系列答案
全能测控期末小状元系列答案| A. | 氧化汞分解成汞和氧气--分子可以再分 | |
| B. | 甘蔗甜,苦瓜苦--不同分子性质不同 | |
| C. | 切洋葱时可闻到刺激性气味--分子在不停运动 | |
| D. | 结冰的水不能流动(0℃以下)--水分子不再运动 |
 某化学兴趣小组的同学对一些小食品的包装方式产生了兴趣.食品装在充满气体的小塑料袋里,这种充气的包装技术主要是为了能使食品较长时间地保质、保鲜.那么,其中充的是什么气体呢?
某化学兴趣小组的同学对一些小食品的包装方式产生了兴趣.食品装在充满气体的小塑料袋里,这种充气的包装技术主要是为了能使食品较长时间地保质、保鲜.那么,其中充的是什么气体呢?【猜想与假设】小文说:该气体可能是CO2、O2、N2、空气.
小航说:不可能含有O2,因为氧气的化学性质比较活泼,会加速食品变质.
【查阅资料】(1)镁条可以在氮气中燃烧,生成物(Mg3N2)与水反应可以产生使湿润的红色石蕊试纸变蓝的物质(NH3).
(2)镁条在空气中燃烧主要生成氧化镁而不是氮化镁.
【进行实验】收集三瓶包装袋内的气体进行实验.请你填写下列表格.
| 猜想 | 验证方法 | 现象 |
| 空气 | 将燃着的木条伸入集气瓶中 | 木条正常燃烧 |
| CO2 | 无明显现象 | |
| N2 | 无明显现象 |
【反思】你认为食品充气包装中,对所充气体的要求是(写两点)
①无毒; ②价廉易得(合理即可).
| A. | 空气中的氧气主要来自于植物的光合作用 | |
| B. | 工业上用分离液态空气的方法制取氧气是分解反应 | |
| C. | 用含有氧元素的物质发生反应才有可能产生氧气 | |
| D. | 用过氧化氢溶液制氧气时不加二氧化锰也能产生氧气 |
| A. | 硫及其化合物与化合价的关系: | B. | 银、铜、铁的金属活动性强弱: | ||
| C. | 物质形成溶液的pH: | D. | 形成溶液时的温度: |

| A. | 都不能 | B. | 只有②③能 | C. | 只有①③能 | D. | 都能 |