题目内容
碳酸钠和硫酸钠的混合物12.4g与100g稀硫酸恰好完全反应,产生2.20g气体求:
(1)原混合物中硫酸钠的质量分数.
(2)反应后溶液中硫酸钠的质量分数(精确到0.1%).
(1)原混合物中硫酸钠的质量分数.
(2)反应后溶液中硫酸钠的质量分数(精确到0.1%).
(1)设原混合物中碳酸钠质量为x,反应生成硫酸钠质量为y
Na2CO3+H2SO4═Na2SO4+CO2↑+H2O
106 142 44
x y 2.20g
=
=
x=5.30g y=7.10g
原混合物中硫酸钠质量=12.4g-5.3g=7.10g
硫酸钠质量分数=
×100%=57.3%
(2)反应后溶液中硫酸钠质量=7.1g+7.1g=14.2g
溶液质量=12.4g+100g-2.20g=110.2g
溶液中硫酸钠质量分数=
×100%=12.9%
答:(1)原混合物中硫酸钠的质量分数为57.3%
(2)反应后溶液中硫酸钠质量分数为12.9%.
Na2CO3+H2SO4═Na2SO4+CO2↑+H2O
106 142 44
x y 2.20g
| 106 |
| x |
| 142 |
| y |
| 44 |
| 2.20g |
x=5.30g y=7.10g
原混合物中硫酸钠质量=12.4g-5.3g=7.10g
硫酸钠质量分数=
| 7.10g |
| 12.4g |
(2)反应后溶液中硫酸钠质量=7.1g+7.1g=14.2g
溶液质量=12.4g+100g-2.20g=110.2g
溶液中硫酸钠质量分数=
| 14.2g |
| 110.2g |
答:(1)原混合物中硫酸钠的质量分数为57.3%
(2)反应后溶液中硫酸钠质量分数为12.9%.

练习册系列答案
相关题目
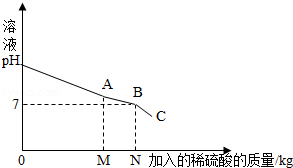
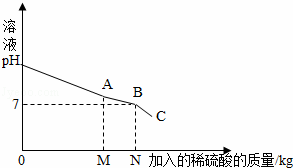
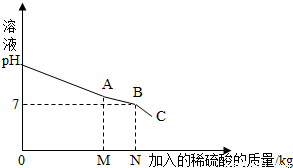
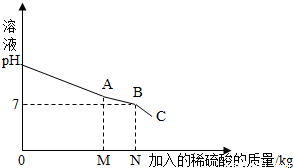
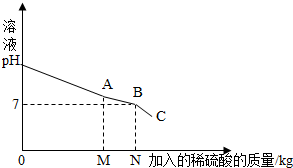 (2013?防城港)我们知道,每次做完实验后,剩余废液不能直接倾倒入排污管,必须回收处理.某班同学实验后收集到含有碳酸钠和氢氧化钠的混合废液5.11Kg,一个兴趣小组用废弃的溶质质量分数为19.6%的硫酸来处理,并回收处理后的溶液.他们向废液中加入稀硫酸时,所得溶液pH与加入的稀硫酸质量的关系曲线如图所示.求:
(2013?防城港)我们知道,每次做完实验后,剩余废液不能直接倾倒入排污管,必须回收处理.某班同学实验后收集到含有碳酸钠和氢氧化钠的混合废液5.11Kg,一个兴趣小组用废弃的溶质质量分数为19.6%的硫酸来处理,并回收处理后的溶液.他们向废液中加入稀硫酸时,所得溶液pH与加入的稀硫酸质量的关系曲线如图所示.求: