题目内容
17.现有三种无色气体A、B、C,三种黑色粉末D、E、F.已知:在一定条件能发生如下反应:①A+D→B②B+D→C③E+D→B+Cu,且F和A都可通过加热一种暗紫色固体获得.请回答下列问题:
(1)请写出以下物质的化学式:
AO2;BCO2;CCO;DC;
(2)加热暗紫色固体生成F和A的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
(3)分别写出反应②、③的化学反应方程式
②CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;③2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
分析 根据反应③D+E→B+Cu分析可知,所以反应③不是化合反应或分解反应,B是无色气体,D、E是黑色粉末,所以反应③置换出铜单质可知是还原反应,所以D、E是氧化铜或木炭中的一种,B是二氧化碳,二氧化碳和黑色粉末D会生成无色气体C,所以D是木炭,C就是一氧化碳,一氧化碳和无色气体A会生成二氧化碳,所以A是氧气,然后将推出的各种物质代入转化关系中验证即可.
解答 解:(1)根据反应③D+E→B+Cu分析可知,所以反应③不是化合反应或分解反应,B是无色气体,D、E是黑色粉末,所以反应③置换出铜单质可知是还原反应,所以D、E是氧化铜或木炭中的一种,B是二氧化碳,二氧化碳和黑色粉末D会生成无色气体C,所以D是木炭,C就是一氧化碳,一氧化碳和无色气体A会生成二氧化碳,且“F和A都可通过加热一种暗紫色固体获得”,“三种黑色粉末D、E、F”,所以暗紫色固体可知是高锰酸钾,气体A是氧气,黑色固体F为二氧化碳.一氧化碳和氧气在点燃的条件下生成二氧化碳,二氧化碳和木炭在高温的条件下生成一氧化碳,木炭和氧化铜在高温的条件下生成铜和二氧化碳,推出的各种物质均满足题中的转化关系,推导合理,所以A是O2,B是CO2;C是CO;D是C.
(2)加热暗紫色固体生成F和A,即高锰酸钾分解,故其化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)根据分析可知,反应②二氧化碳和木炭在高温的条件下生成一氧化碳、反应③木炭和氧化铜在高温的条件下生成铜和二氧化碳,故其化学反应方程式分别为:
②CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;③2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
故答案为:
(1)O2; CO2;CO; C;(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;(3)CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO; 2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 我国稀土元素储量、生产规模及出口量居世界首位.铈(Ce)是一种常见的稀土元素,下列有关说法不正确的是( )
我国稀土元素储量、生产规模及出口量居世界首位.铈(Ce)是一种常见的稀土元素,下列有关说法不正确的是( )| A. | 原子序数是58 | B. | 相对原子质量是140.1g | ||
| C. | 质子数为58 | D. | 铈元素是金属元素 |
| A. | H | B. | O2 | C. | 2H2O | D. | He |
| A. | 滴水成冰 | B. | 玻璃破碎 | C. | 酒精燃烧 | D. | 西瓜榨汁 |
| A. | 海水晒盐 | B. | 酒精挥发 | C. | 菜刀生锈 | D. | 分离空气制氧气 |
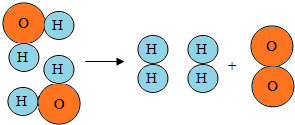 写出从如图水分子分解示意图中获得的信息,(至少写出三条)
写出从如图水分子分解示意图中获得的信息,(至少写出三条)