题目内容
(2006?海南)完成下面实验报告:
实验内容:铁和铜金属活动性比较
实验内容:铁和铜金属活动性比较
| 实验操作 | 现 象 | 结论及化学方程式 |
| 向试管中加人约1/4试管CuSO4溶液将-块银白色铁片插入溶液中,一会儿后取出,观察现象. | 溶液颜色变浅 铁片表面出现红色 溶液颜色变浅 铁片表面出现红色 | 铁能把溶液中的Cu2+置换出来,说明铁比铜活泼, Fe+CuSO4═FeSO4+Cu 铁能把溶液中的Cu2+置换出来,说明铁比铜活泼, Fe+CuSO4═FeSO4+Cu |
分析:根据金属活动性顺序表可以知道金属铁的活动性比铜的强,结合金属活动性顺序的应用可以知道:铁能够把铜从其溶液中置换出来,可以据此来判断并解答该题.
解答:解:根据金属活动性顺序可以知道铁的活动性比铜的强,所以若将铁片插入硫酸铜溶液中,铁会把铜置换出来,即在铁的表面会产生红色物质,从而可以得出铁活动性比铜强的结论.
故答案为:
故答案为:
| 现 象 | 结论与化学方程式 |
| 溶液颜色变浅 铁片表面出现红色 | 铁能把溶液中的Cu2+ 置换出来,说明铁比铜活泼, Fe+CuSO4═FeSO4+Cu |
点评:熟练掌握金属活动性顺序及其应用,并能够利用金属活动性顺序的应用及题给的信息来判断置换反应能否发生,进而判断出它们的活动性顺序.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
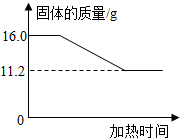 (2006?嘉兴)完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数.
(2006?嘉兴)完成下列研究性学习的有关内容:探究氯酸钾和二氧化锰混合物中氯酸钾的质量分数.