题目内容
2. 水是生命的源泉,也是不可缺少的资源.
水是生命的源泉,也是不可缺少的资源.(1)某矿泉水的主要矿物质成分及含量如下表:
| 成分 | Ca | K | Mg | Na |
| 含量(mg/L) | ≥4 | ≥0.4 | ≥0.5 | ≥0.8 |
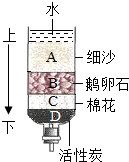
(2)如图是某同学自制的简易净水器.其中放置物质的顺序有错误,为使净水效果最佳,请仿照自来水生产流程帮他按由上到下的顺序重新排列BADC(填字母).
(3)下列做法会造成水体污染的有A(填序号).
A.工业废水直接排放 B.生活污水集中处理后排放
C.禁止使用含磷洗衣粉 D.合理使用化肥、农药
(4)目前,人类以化石燃料为主要能源,化石燃料有煤、石油和天然气,它们都属于不可再生(填“可再生”或“不可再生”)能源.天然气的主要成分是甲烷(CH4),写出甲烷在空气中完全燃烧的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
分析 (1)物质的组成常用元素来描述;根据硬水、软水与肥皂水反应的现象不同来鉴别;
(2)根据净化水的顺序分析;
(3)根据水的污染源分析;
(4)根据化石能源的种类及形成特点分析回答.根据甲烷燃烧的反应写出反应的方程式.
解答 解:(1)物质的组成常用元素来描述,这里的这里Ca、K、Mg、Na是指元素;生活中可用肥皂水来区别硬水和软水,泡沫多的为软水,泡沫少的为硬水;
(2)按由上到下的顺序重新排列应该是:用小卵石除去较大的颗粒,再用石英砂除去较小的颗粒,再用活性炭除去色素和异味,最后是蓬松棉,起支撑作用.故填:BADC;
(3)污染的水的危害性比较大,我们要防止水的污染.生活污水处理后排放,禁止使用含磷洗衣粉,合理使用化肥、农药不会造成水的污染;工业废水直接排放会造成水的污染.;
(4)化石燃料有煤、石油和天然气,是由古代的生物遗骸经过一系列的变化而形成的,它们都属于不可再生能源;天然气中甲烷在空气中完全燃烧,生成了二氧化碳和水,反应的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
故答案为:(1)元素;肥皂水;
(2)BADC;
(3)A;
(4)天然气;不可再生;CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
点评 本题难度不大,熟练掌握常见物质的性质、用途、组成及化学式的书写是正确解答此类题的关键所在.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
5.下列应用对应的化学方程式及基本反应类型正确的是 ( )
| A. | 用熟石灰中和硫酸厂的废水Ca(OH)2+H2SO4═CaSO4+2H2O 中和反应 | |
| B. | 生石灰作干燥剂CaO+H2O═Ca(OH)2 化合反应 | |
| C. | 用氢氧化钠溶液吸收二氧化碳2NaOH+CO2═Na2CO3+H2O 复分解反应 | |
| D. | 高炉炼铁4CO+Fe3O4═4CO2+3Fe 置换反应 |
13.小刚、小军、小红对一久置的NaOH白色粉末的成分进行探究并测定其成分的含量.
(一)成分的确定
三位同学都作出以下的猜想:
①可能是NaOH; ②可能是Na2CO3; ③可能是NaOH与Na2CO3的混合物.
(1)做出②③猜想的依据是CO2+2NaOH═Na2CO3+H2O(用化学方程式表示)
(2)为了验证①②③猜想,他们分别做了下面的实验.
小刚取少量白色粉末于试管中,再滴加稀HCl,有气泡产生,由此可推出白色粉末中一定含有Na2CO3,肯定猜想①(填序号)是错误的.
小军又取少量白色粉末溶于水,向所得溶液中滴加酚酞试液,溶液变为红色.由此小军结合小刚的实验,认为猜想③是正确的.小红却认为小军的所得结论不确切,因为Na2CO3显碱性也会使酚酞试液变红.
(3)为探究白色粉末是否含有NaOH,小红设计了如图1所示实验方案:

①沉淀B的化学式为CaCO3.
②在操作1中要用到玻璃棒,其作用是搅拌;在操作2中,除要用到铁架台(带铁圈)、烧杯、滤纸、玻璃棒外,还需补充的玻璃仪器是漏斗.
③小刚认为小红的这个方案也有问题,理由是Na2CO3与Ca(OH)2反应后也有NaOH生成. 但只要稍加改进,就可以证明粉末中还含有NaOH,则小刚改进的方法是将滴加澄清石灰水改为过量的CaCl2(或Ba(NO3)2 或Ca(NO3)2或BaCl2).小刚对小红的实验作了正确的改进后进行了实验,实验现象和小红的一致,由此确定猜想③是正确的.
(二)各成分含量的测定
三位同学利用电子天平共同作了如图2所示测定实验.
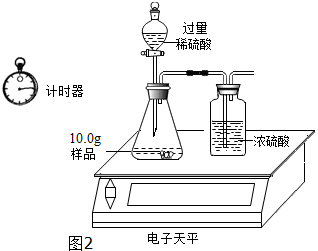
实验数据记录如表:
(4)写出锥形瓶中发生反应化学方程式:2NaOH+H2SO4═Na2SO4+2H2O;Na2CO3+H2SO4═Na2SO4+H2O+CO2↑.
(5)试通过分析表中数据计算出混合物中试样中各成份的质量分数,NaOH47%,Na2CO353%.
(三)实验反思:
(1)有同学提出按上述实验所测得试样中Na2CO3质量分数会偏小,该同学的理由是CO2密度比空气大,会有CO2残留在装置中,造成最终测得的质量偏大,测得生成的CO2质量偏小.(或浓硫酸会吸收空气中的水份,造成最终测得的质量偏大,测得生成的CO2质量偏小.)(实验操作均正确).
(2)根据反应的化学方程式分析,NaOH部分变质或全部变质,与没有变质的NaOH相比,中和反应时消耗硫酸的量相等(填“相等”、“大于”或“小于”)
(一)成分的确定
三位同学都作出以下的猜想:
①可能是NaOH; ②可能是Na2CO3; ③可能是NaOH与Na2CO3的混合物.
(1)做出②③猜想的依据是CO2+2NaOH═Na2CO3+H2O(用化学方程式表示)
(2)为了验证①②③猜想,他们分别做了下面的实验.
小刚取少量白色粉末于试管中,再滴加稀HCl,有气泡产生,由此可推出白色粉末中一定含有Na2CO3,肯定猜想①(填序号)是错误的.
小军又取少量白色粉末溶于水,向所得溶液中滴加酚酞试液,溶液变为红色.由此小军结合小刚的实验,认为猜想③是正确的.小红却认为小军的所得结论不确切,因为Na2CO3显碱性也会使酚酞试液变红.
(3)为探究白色粉末是否含有NaOH,小红设计了如图1所示实验方案:

①沉淀B的化学式为CaCO3.
②在操作1中要用到玻璃棒,其作用是搅拌;在操作2中,除要用到铁架台(带铁圈)、烧杯、滤纸、玻璃棒外,还需补充的玻璃仪器是漏斗.
③小刚认为小红的这个方案也有问题,理由是Na2CO3与Ca(OH)2反应后也有NaOH生成. 但只要稍加改进,就可以证明粉末中还含有NaOH,则小刚改进的方法是将滴加澄清石灰水改为过量的CaCl2(或Ba(NO3)2 或Ca(NO3)2或BaCl2).小刚对小红的实验作了正确的改进后进行了实验,实验现象和小红的一致,由此确定猜想③是正确的.
(二)各成分含量的测定
三位同学利用电子天平共同作了如图2所示测定实验.

实验数据记录如表:
| 称 量 项 目 | 称 量 时 间 | 质量(g) |
| 试样 | 10.00 | |
| 装置+稀硫酸质量 | 241.20 | |
| 装置+稀硫酸质量+试样 | 反应开始后15秒 | 249.20 |
| 装置+稀硫酸质量+试样 | 反应开始后35秒 | 249.00 |
| 装置+稀硫酸质量+试样 | 反应开始后55秒 | 249.00 |
(5)试通过分析表中数据计算出混合物中试样中各成份的质量分数,NaOH47%,Na2CO353%.
(三)实验反思:
(1)有同学提出按上述实验所测得试样中Na2CO3质量分数会偏小,该同学的理由是CO2密度比空气大,会有CO2残留在装置中,造成最终测得的质量偏大,测得生成的CO2质量偏小.(或浓硫酸会吸收空气中的水份,造成最终测得的质量偏大,测得生成的CO2质量偏小.)(实验操作均正确).
(2)根据反应的化学方程式分析,NaOH部分变质或全部变质,与没有变质的NaOH相比,中和反应时消耗硫酸的量相等(填“相等”、“大于”或“小于”)
10.如表列出了一些粒子的结构示意图,请回答问题:
(1)具有相对稳定结构的粒子是DE(用ABCDE表示);
(2)表格中共有3种原子;
(3)在化学反应中容易失去电子的粒子是AC(用ABCDE表示).
| A | B | C | D | E |
 |  |  |  |  |
(2)表格中共有3种原子;
(3)在化学反应中容易失去电子的粒子是AC(用ABCDE表示).
17.某同学对所学部分化学知识归纳如下,其中正确的一组是
( )
| A | 微粒观点解释现象 | B | 物质及其应用 |
| 花香四溢--微粒在不断运动 热胀冷缩--微粒大小发生变化 | 干冰--人工降雨 食盐--促进冰雪融化 | ||
| C | 化学与生活 | D | 元素与人体健康 |
| 洗面奶洗脸--乳化 油锅起火--用水浇灭 | 缺铁--易引起贫血 缺碘--易得侏儒症 |
| A. | A | B. | B | C. | C | D. | D |
7. 利用如图所示装置测定某含菱铁矿的矿石样品中碳酸亚铁的质量分数(杂质不含铁元素且在实验过程中不发生任何变化),实验数据记录在下表中.
利用如图所示装置测定某含菱铁矿的矿石样品中碳酸亚铁的质量分数(杂质不含铁元素且在实验过程中不发生任何变化),实验数据记录在下表中.
提示:FeCO3 $\frac{\underline{\;高温\;}}{\;}$FeO+CO2↑,CO+FeO$\frac{\underline{\;高温\;}}{\;}$Fe+CO2
下列判断正确的是( )
 利用如图所示装置测定某含菱铁矿的矿石样品中碳酸亚铁的质量分数(杂质不含铁元素且在实验过程中不发生任何变化),实验数据记录在下表中.
利用如图所示装置测定某含菱铁矿的矿石样品中碳酸亚铁的质量分数(杂质不含铁元素且在实验过程中不发生任何变化),实验数据记录在下表中.提示:FeCO3 $\frac{\underline{\;高温\;}}{\;}$FeO+CO2↑,CO+FeO$\frac{\underline{\;高温\;}}{\;}$Fe+CO2
| 实验前 | 实验后 | |
| 硬质玻璃管(含样品) | 160.6g | 154.6g |
| 说 明 | ①空硬质玻璃管质量为l40.6g ②含铁各物质反应完全 | |
| A. | 一氧化碳还原氧化亚铁的反应属于置换反应 | |
| B. | 充分反应后,玻璃管及其中物质的总质量较反应前减少6g,该质量为参加反应的碳酸亚铁中碳酸根的质量 | |
| C. | 矿石样品中含碳酸亚铁的质量为11.6g | |
| D. | 实验结束后盛有澄清石灰水的试管的总质量比反应前的总质量增加了4.4g |
11.下列说法错误的是( )
| A. | 化学反应中,反应物的总质量等于生成物的总质量 | |
| B. | 镁条燃烧后,生成物质量大于镁条质量 | |
| C. | 反应物和生成物分子个数一定相等 | |
| D. | 化学反应前后,元素种类没变 |
12.下列物质中都含有( )
H2O H2O2 H2SO4 H2CO3.
H2O H2O2 H2SO4 H2CO3.
| A. | 氢元素 | B. | 2个氢原子 | C. | 氢分子 | D. | 氢气 |