题目内容
18.为了测定黄铜样品中铜的质量分数,某化学小组进行了如下实验: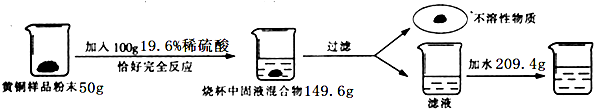
(1)配制上述质量分数为19.6%的稀硫酸,需要质量分数为98%的浓硫酸的质量是20g;
(2)发生反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑;
(3)根据已知条件列出求解50g该黄铜样品中锌的质量(X)的比例式为$\frac{65}{x}$=$\frac{98}{100g×19.6%}$;
(4)该黄铜样品中铜的质量分数是74%;
(5)向过滤后所得滤液中加入209.4g水,则最终所得溶液中溶质的质量分数10%;
(6)若工业上用125t含Cu2S74%的辉铜矿炼制该黄铜,则理论上能炼制出黄铜的质量为100t.
分析 (1)根据溶液稀释前后溶质质量分数不变进行分析;
(2)根据锌和稀硫酸反应生成硫酸锌和氢气进行分析;
(3)根据锌和稀硫酸反应生成硫酸锌和氢气,依据参加反应的硫酸质量计算参加反应的锌的质量;
(4)根据计算出的锌的质量计算铜的质量分数;
(5)根据化学方程式计算生成的硫酸锌,然后计算最终所得溶液中溶质的质量分数;
(6)根据铜元素守恒计算炼制出的黄铜质量.
解答 解:(1)需要质量分数为98%的浓硫酸的质量是:$\frac{100g×19.6%}{98%}$=20g;
(2)锌和稀硫酸反应生成硫酸锌和氢气化学方程式为:Zn+H2SO4=ZnSO4+H2↑;
(3)设参加反应的锌的质量为x,生成硫酸锌的质量为y,生成氢气质量为z
Zn+H2SO4=ZnSO4+H2↑
65 98 161 2
x 100g×19.6% y z
$\frac{65}{x}$=$\frac{98}{100g×19.6%}$=$\frac{161}{y}$=$\frac{2}{z}$
x=13g
y=32.2g
z=0.4g
(4)黄铜样品中铜的质量分数是:$\frac{50g-13g}{50g}$×100%=74%;
(5)最终所得溶液中溶质的质量分数为:$\frac{32.2g}{100g+13g+209.4g-0.4g}$×100%=10%;
(6)理论上能炼制出黄铜的质量为:$\frac{125t×74%×\frac{128}{160}×100%}{74%}$=100t.
故答案为:(1)20g;(2)Zn+H2SO4=ZnSO4+H2↑;
(3)$\frac{65}{x}$=$\frac{98}{100g×19.6%}$;
(4)74%;
(5)10%;
(6)100t.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性.


| A. | 化学式为NH3 | B. | 属于混合物 | ||
| C. | 氮元素和氢元素的质量比为3:1 | D. | 氢元素的质量分数$\frac{1}{17}$×100%=5.9% |
(1)碳原子的结构示意为
 ,碳原子的核电荷数为6.
,碳原子的核电荷数为6.(2)根据表1提供的信息,填写有关含碳物质的对应特性.
表1
| 物质用途 | 金刚石切割玻璃 | 石墨作电极 | 活性炭净水 |
| 对应特征 | 硬度大 | ②能导电 | 具有强的吸附性 |
A.液态二氧化碳汽化后不会污染档案资料
B.二氧化碳可覆盖在燃烧物表面,隔绝空气
C.液态二氧化碳汽化时吸热,降低了可燃物的着火点
(4)我们知道酸类物质可使紫色石蕊试液变红,小冬为了探究H2CO3具有酸性,而CO2不具有酸性,他设计了如图2的实验.请写出将观察到的现象:

现象:试纸不变色 现象:试纸变红
(5)过多的二氧化碳加剧了“温室效应”,写出一条减少二氧化碳排放的建议绿色出行、植树造林等.
(6)目前,人类以化石燃料为主要能源.化石燃料有煤、石油和天然气,它们都属于不可再生(填“可再生”或“不可再生”)能源.
| A. | 磷在空气中燃烧,反应剧烈,产生大量白雾 | |
| B. | 铁丝在氧气中燃烧,火星四射,生成黑色固体 | |
| C. | 蜡烛在空气中燃烧,发出耀眼的白光,生成白色固体 | |
| D. | 硫在氧气中燃烧,火焰呈蓝紫色,生成有刺激性气味的气体 |
| 物质 | 杂质 | 除杂质所用试剂和方法 | |
| A | H2 | O2气体 | 先通过灼热的铜网,再通过浓硫酸 |
| B | KNO3溶液 | AgNO3溶液 | 先加入过量KCl溶液,再过滤 |
| C | KCl固体 | KClO3固体 | 加入少量MnO2加热 |
| D | FeSO4溶液 | CuSO4溶液 | 先加过量Fe粉,再过滤 |
| A. | A | B. | B | C. | C | D. | D |