题目内容
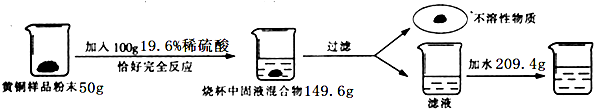
17.乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属,乙炔由碳化钙(块状固体,化学式为CaC2)与水反应生成,同时生成一种白色固体.【查阅资料】电石主要成分为碳化钙(CaC2),它没有可燃性.
【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下几种可能:
猜想一:CaO; 猜想二:CaCO3; 猜想三:Ca(OH)2.
他的依据是根据质量守恒定律.
【交流反思】经过同学们交流讨论,认为猜想一不成立.理由是:氧化钙与水反应也生成氢氧化钙.
【进行实验】
(一)取少量白色固体放入试管中,滴加稀盐酸,没有观察到气泡放出,证明猜想二不成立.
(二)取少量白色固体加入到水中,取上层清液,通入二氧化碳气体,有白色浑浊出现,证明猜想三成立.该反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O.
结论:白色固体是Ca(OH)2.
【拓展应用】某市一辆满载电石的货车遇大雨引发熊熊大火,其中的可燃物是乙炔,且该反应放出大量热,使可燃物达到着火点.
【交流反思】通过上述实验可知,电石在保存和运输时的注意事项防止与水接触.
分析 【做出猜想】
根据质量守恒定律可知,白色固体可能是氧化钙,或碳酸钙,或氢氧化钙;
【交流反思】
氧化钙能和水反应生成氢氧化钙;
【进行实验】
碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳能使澄清的石灰水变浑浊;
根据反应物和生成物利用质量守恒定律写化学方程式.
【拓展应用】据物质燃烧的条件回答;
【交流反思】利用电石与水反应的性质分析.
解答 解:
【做出猜想】
猜想一:CaO;猜想二CaCO3:;猜想三:Ca(OH)2.
他的依据是根据质量守恒定律;
故填:CaCO3;根据质量守恒定律;
【交流反思】
经过同学们交流讨论,认为猜想一不成立.否定猜想一的理由是:CaO能与水反应.
故填:氧化钙与水反应也生成氢氧化钙.
【进行实验】
(一)取少量白色固体放入试管中,滴加稀盐酸,没有观察到气泡放出,证明猜想二不成立.
故填:气泡放出.
(二)取少量白色固体加入到水中,取上层清液,通入二氧化碳气体,有白色沉淀出现,证明猜想三成立.二氧化碳与澄清的石灰水反应的化学方程式Ca(OH)2+CO2=CaCO3↓+H2O
【拓展应用】电石无可燃性,但电石与水反应生成的乙炔气体具有可燃性,且这一反应放出热量,使可燃物的温度达到着火点.
【交流反思】据题可知电石遇水反应生成可燃性气体乙炔,存在危险,所以电石在保存和运输时的注意事项是防止与水接触.
故答案为:
【做出猜想】
CaCO3; 根据质量守恒定律;
【交流反思】氧化钙与水反应也生成氢氧化钙;
【进行实验】
(-)有气泡冒出;
(二)二氧化碳气体; Ca(OH)2+CO2=CaCO3↓+H2O;
【拓展应用】乙炔或C2H2;着火点;
【交流反思】防止与水接触;
点评 化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,并有助于提高观察、实验能力.所以,对化学实验不仅要认真观察,还应掌握观察实验现象的方法.

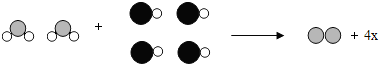
| A. | 反应前后元素种类发生了改变 | |
| B. | 1个X分子中有三个原子 | |
| C. | 两种反应物之间的质量比为1:2 | |
| D. | 各元素的化合价在反应前后均未改变 |
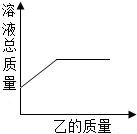 在一定质量的甲溶液中逐渐加入乙至过量,反应过程中溶液的总质量与加入乙的质量的关系如下图所示,表中物质能用图所示曲线表示的是( )
在一定质量的甲溶液中逐渐加入乙至过量,反应过程中溶液的总质量与加入乙的质量的关系如下图所示,表中物质能用图所示曲线表示的是( ) | 序号 | 甲 | 乙 |
| ① | 稀盐酸 | 碳酸钠溶液 |
| ② | 稀盐酸 | 铁锈 |
| ③ | 稀硫酸 | 锌粒 |
| ④ | NaOH溶液 | 紫色石蕊试液 |
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②③ |
| A. | 将铝粉涂在铁器的表面以保护铁 | B. | 真金不怕火炼 | ||
| C. | 钨在高温下不易熔化 | D. | 燃烧镁做照明弹 |