题目内容
10.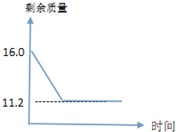 小明用加热氯酸钾和二氧化锰混合物的方法制取氧气,反应前氯酸钾和二氧化锰总质量16.0克,完全反应后剩余固体的总质量如图所示.求:
小明用加热氯酸钾和二氧化锰混合物的方法制取氧气,反应前氯酸钾和二氧化锰总质量16.0克,完全反应后剩余固体的总质量如图所示.求:(1)反应产生氧气的质量为4.8克;
(2)参加反应的氯酸钾的质量为多少?(写出解题过程)
分析 (1)依据质量守恒定律反应前后固体的质量之差即为反应中生成的氧气质量;
(2)利用氧气的质量结合方程式即可求出氯酸钾的质量.
解答 解:(1)根据质量守恒定律,生成氧气的质量=16 g-11.2g=4.8 g
(2)设原混合物中氯酸钾的质量为x,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
x 4.8g
$\frac{245}{96}=\frac{x}{4.8g}$
x=12.25g
答:参加反应的氯酸钾的质量为12.25g.
点评 此题是化学方程式的计算考查题,解题的关键是根据质量守恒定律,由反应前后固体物质质量差即反应所产生氧气的质量.

练习册系列答案
相关题目
1.如表是鉴别方法不能把待鉴别的物质区分开的是( )
| 待鉴别的物质 | 鉴别方法 | |
| A | 蒸馏水和海水 | 加AgNO3溶液 |
| B | 硫酸铵溶液和硝酸钾溶液 | 加氯化钡溶液 |
| C | 羊毛面料和腈纶面料 | 抽丝点燃闻气味 |
| D | 氢氧化钠溶液和碳酸钠溶液 | 加无色酚酞试液 |
| A. | A | B. | B | C. | C | D. | D |
18.每年的5月13 日是世界无烟日,香烟的成分很复杂,燃烧产生的烟气中含有许多强致癌物质和有害物质,其中对人体危害最大的分别是尼古丁(化学式为C10H14N2)、焦油、一氧化碳等,下列说法错误的是( )
| A. | 吸烟严重危害身心健康 | |
| B. | 尼古丁中碳、氢、氧三种元素质量比为60:7:14 | |
| C. | 尼古丁中含有10个碳原子,14个氢原子和2个氮原子 | |
| D. | 一氧化碳能与血液里的血红蛋白结合,故而有剧毒 |
5.下列说法中,符合实验室化学药品取用规则的是( )
| A. | 为了节约药品,用剩的药品可放回原瓶 | |
| B. | 如果没有说明用量,应该按最少量取,液体取4-5mL | |
| C. | 用剩的药品,只要不是危险药品就可以拿出实验室 | |
| D. | 闻气体药品时,应用手轻轻煽动气体,使少量气体飘入鼻孔 |
15.下列实验现象或实验原理正确的是( )
| A. | 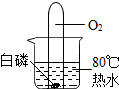 白磷始终不燃烧 | B. | 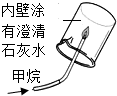 验证甲烷燃烧生成二氧化碳和水 | ||
| C. | 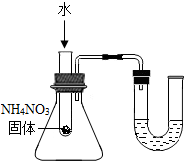 U形管内液面左高右低 | D. | 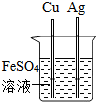 验证Fe、Cu、Ag的金属或定性强弱 |
2.下列关于反应的描述,反应方程式及反应类型完全正确的是( )
| A. | 小苏打受热分解:NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O 化合反应 | |
| B. | 铁丝在氧气中燃烧:4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 分解反应 | |
| C. | 检验食盐中存在氯离子:NaCl+AgNO3═NaNO3+AgCl↓ 复分解反应 | |
| D. | 将铁片投入足量的稀盐酸中:2Fe+6HCl═2FeCl3+3H2↑ 置换反应 |