题目内容
19.A、B、C、D、E、F、G为初中化学常见物质,它们之间有如甲图所示的反应关系(部分反应物及产物已略去,图中“→”表示两者之间能转化),已知B是常用的建筑材料,D常温下为液体,C和G之间也能发生反应,回答下列问题: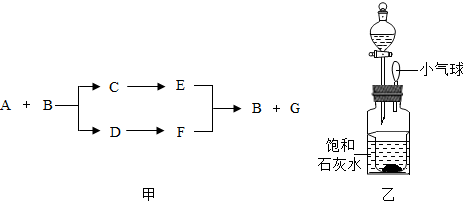
(1)G物质的俗称为烧碱,E的化学式Na2CO3,F的化学式Ca(OH)2.
(2)C在生活中的重要应用有灭火(举一例).
(3)D→F的化学方程式为CaO+H2O=Ca(OH)2.
(4)从上述物质中选出合适的物质,利用乙图所示装置进行实验,将分液漏斗内的液体放入小烧杯中,观察到饱和石灰水变浑浊,写出符合要求的组合(写两组即可)稀盐酸、碳酸钙、水、氢氧化钠.
分析 根据人体所需的营养素:水、油脂、糖类、蛋白质、无机盐、维生素,D是人体所需营养素之一,可以通过A和B反应生成,所以D就是水,A、B反应生成的水和C经过一系列的反应会生成B和G,G和C又会反应,猜想B是碳酸钙,A是盐酸,C是二氧化碳,F是氢氧化钙,E是碳酸钠,氢氧化钙和碳酸钠反应生成的碳酸钙和氢氧化钠,氢氧化钠会与二氧化碳反应,将各种物质代入转换关系中进行验证,
(1)根据推导出的物质进行分析,
(2)根据分析推测C物质,进行分析用途;
(3)根据推导出的反应物、生成物书写方程式.
(4)根据氢氧化钙的溶解度受温度变化的影响进行分析,
解答 解:人体所需的营养素:水、油脂、糖类、蛋白质、无机盐、维生素,D是人体所需营养素之一,可以通过A和B反应生成,所以D就是水,A、B反应生成的水和C经过一系列的反应会生成B和G,G和C又会反应,猜想B是碳酸钙,A是盐酸,C是二氧化碳,F是氢氧化钙,E是碳酸钠,氢氧化钙和碳酸钠反应生成的碳酸钙和氢氧化钠,氢氧化钠会与二氧化碳反应,各种物质都满足转换关系,所以A是盐酸,B是碳酸钙,C是二氧化碳,D是水,E是碳酸钠,F是氢氧化钙,G是氢氧化钠,代入检验,符合题意.
(1)根据分析,G是氢氧化钠,E是碳酸钠,F是氢氧化钙,故G物质的俗称为烧碱、火碱、苛性钠,E的化学式Na2CO3,F的化学式Ca(OH)2.
(2)根据分析,C是二氧化碳,不助燃,不可燃,密度比空气大,故C在生活中的重要应用有:灭火.
(3)根据分析,D是水,F是氢氧化钙,反应D→F,即氧化钙与水反应生成氢氧化钙,故其化学方程式为CaO+H2O=Ca(OH)2.
(4)氢氧化钙的溶解度随温度的升高而减小,饱和的石灰水出现浑浊,可能与二氧化碳反应生成了碳酸钙,也可能溶液的温度升高了,溶解度减小,氢氧化钙晶体析出,故答案为:
| 物质 序号 | ① | ② | ③ | ④ |
| 液体 | HCl | HCl | H2O | |
| 固体 | CaCO3 | Na2CO3 | NaOH |
(1)烧碱、火碱、苛性钠,Na2CO3,Ca(OH)2.(2)灭火.
(3)CaO+H2O=Ca(OH)2.(4)稀盐酸和碳酸钙、水和氢氧化钠或稀盐酸和碳酸钠等.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可.通过该题,需要掌握氢氧化钙的溶解度受温度变化的影响.

 名校课堂系列答案
名校课堂系列答案| A. | 该反应是置换反应 | B. | 金属R可能是铁 | ||
| C. | 金属R活动性比Cu强 | D. | 反应前后R的化合价保持不变 |
| A. | 原子中一定含有质子、中子和电子三种微粒 | |
| B. | 饱和溶液升高温度后都会变成不饱和溶液 | |
| C. | pH<7的溶液呈酸性,pH值越小,溶液的酸性越强 | |
| D. | 根据质量守恒定律:3克碳在10克氧气中充分燃烧生成13克二氧化碳 |
| A. |  辣椒 | B. |  牛肉 | C. |  牛奶 | D. |  米饭 |
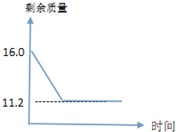 小明用加热氯酸钾和二氧化锰混合物的方法制取氧气,反应前氯酸钾和二氧化锰总质量16.0克,完全反应后剩余固体的总质量如图所示.求:
小明用加热氯酸钾和二氧化锰混合物的方法制取氧气,反应前氯酸钾和二氧化锰总质量16.0克,完全反应后剩余固体的总质量如图所示.求:
 如图是关于氧气的制取与性质实验装置图.回答下列问题:
如图是关于氧气的制取与性质实验装置图.回答下列问题: ”表示氧原子,“
”表示氧原子,“ ”表示氢原子.请回答下列问题.
”表示氢原子.请回答下列问题.