题目内容
9.有一包固体A,可能含有Cu(OH)2、AgCl、NaOH、Na2CO3、CaCl2中的几种,取少量的A做如下实验,现象如图所示.
根据实验过程中的现象判断:
(1)气体D是CO2(填化学式,下同).
(2)生成蓝色溶液F的化学方程式是Cu(OH)2+2HCl=CuCl2+2H2O.
(3)混合物A中一定存在的可溶物是Na2CO3.
(4)滤液B中,可能存在的溶质是NaOH.若要证明该物质是否存在,首先应加入的试剂是过量的氯化钙或氯化钡溶液,然后再滴加无色酚酞.
分析 根据氯化银沉淀不溶于酸,氢氧化铜沉淀溶于酸生成氯化铜,碳酸钠会与酸反应生成二氧化碳气体,碳酸根离子和钙离子会生成碳酸钙沉淀等知识进行分析.
解答 解:氯化银沉淀不溶于酸,氢氧化铜沉淀溶于酸生成氯化铜,碳酸钠会与酸反应生成二氧化碳气体,碳酸根离子和钙离子会生成碳酸钙沉淀.
滤液B加入适量的盐酸,产生气体D,所以B中含有碳酸钠,A中一定含有碳酸钠,碳酸钠和氯化钙会生成碳酸钙沉淀,但是沉淀C中加盐酸,没有气泡产生,说明C中不含碳酸钙,所以A中一定不含氯化钙,沉淀C中加入过量的盐酸,会生成蓝色溶液和沉淀G,所以A中一定含有氢氧化铜和氯化银,题中的现象不能确定A中是否含有氢氧化钠.逸出:
(1)气体D是二氧化碳,故填:CO2;
(2)生成蓝色溶液F的反应是氢氧化铜和盐酸反应生成氯化铜和水,故反应的化学方程式是:Cu(OH)2+2HCl=CuCl2+2H2O;
(3)通过推导可知,混合物A中一定含有:Cu(OH)2、AgCl、Na2CO3;只有碳酸钠可溶;故填:Na2CO3;
(4)要验证是否含有氢氧化钠,需要排除碳酸钠的干扰,所以取少量滤液B于试管中,加入过量的氯化钙溶液,然后滴加酚酞,溶液变红色,证明含有氢氧化钠,不变色,证明不含氢氧化钠;故填:过量的氯化钙或氯化钡溶液.
点评 本题为框图型物质推断题,完成此类题目,可以依据题干提供的信息,结合框图,找准解题的突破口,直接得出物质的化学式,然后顺推或逆推或由两边向中间推得出其他物质的化学式.

练习册系列答案
相关题目
19.生活中常见的下列物质中,属于纯净物的是( )
| A. | 硬水 | B. | 纯碱 | C. | 生铁 | D. | 青铜 |
20.离子检验的常用方法有三种:
下列离子检验的方法不合理的是( )
| 检验方法 | 沉淀法 | 显色法 | 气体法 |
| 含义 | 反应中有沉淀产生 | 反应中有颜色变化 | 反应中有气体产生 |
| A. | H+--沉淀法 | B. | NH4+--气体法 | C. | Cu2+--显色法 | D. | CO32---气体法 |
17.下列对一些事实的解释不正确的是( )
| 事实 | 解释 | |
| A | 木炭燃烧能生成二氧化碳或一氧化碳 | 反应物的质量不同生成物可能不同 |
| B | 双氧水能杀菌消毒而水则不能 | 两种物质的分子构成不同 |
| C | 氯化铜与氢氧化钙两溶液间的反应速率比两固体间的反应快 | 参加反应的粒子在溶液中接触面积比在固体中接触面积大 |
| D | 电解水得到氢气和氧气 | 水由氢分子和氧分子构成 |
| A. | A | B. | B | C. | C | D. | D |
4.下列变化属于化学变化的是( )
| A. | 夜幕降临,城市霓虹灯通电后发出美丽的亮光 | |
| B. | 青铜受热熔化后浇铸成各种形状的工艺品 | |
| C. | 自来水通过蒸馏变成可饮用的瓶装蒸馏水 | |
| D. | 城市自来水的净化过程为:取水→沉降→过滤→吸附→消毒→配水.其中的消毒过程 |
14.下列物质的用途中,利用其物理性质的是( )
| A. | 氧气用于气焊 | B. | 生石灰用作干燥剂 | ||
| C. | 硫酸用于处理碱性废液 | D. | 汽油洗涤衣服上的油污 |
18.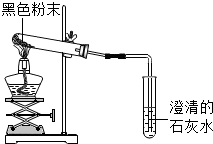 化学小组同学帮助老师整理实验室时,发现一包黑色粉末,老师告诉他们这包粉末是炭粉、铁粉、氧化铜中的两种,为了探究这包黑色粉末的成分,小组同学进行了如下实验:
化学小组同学帮助老师整理实验室时,发现一包黑色粉末,老师告诉他们这包粉末是炭粉、铁粉、氧化铜中的两种,为了探究这包黑色粉末的成分,小组同学进行了如下实验:
【查阅资料】金属氧化物能与酸溶液反应生成可溶性的盐和水.
【提出猜想】猜想一:可能是炭粉和铁粉;猜想二:可能是铁粉和氧化铜
猜想三:可能是炭粉和氧化铜.
【实验验证】
实验一:
实验二:为了验证猜想三成立,小组同学设计了如图实验.
(1)实验中观察到的现象是黑色粉末变红色,澄清石灰水变浑浊,写出两种黑色粉末发生反应的化学方程式2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
(2)小红同学认为该装置设计存在问题,你认为该装置缺陷后是没有尾气处理,若产生的气体中含有一氧化碳会污染空气.
 化学小组同学帮助老师整理实验室时,发现一包黑色粉末,老师告诉他们这包粉末是炭粉、铁粉、氧化铜中的两种,为了探究这包黑色粉末的成分,小组同学进行了如下实验:
化学小组同学帮助老师整理实验室时,发现一包黑色粉末,老师告诉他们这包粉末是炭粉、铁粉、氧化铜中的两种,为了探究这包黑色粉末的成分,小组同学进行了如下实验:【查阅资料】金属氧化物能与酸溶液反应生成可溶性的盐和水.
【提出猜想】猜想一:可能是炭粉和铁粉;猜想二:可能是铁粉和氧化铜
猜想三:可能是炭粉和氧化铜.
【实验验证】
实验一:
| 实验操作 | 实验现象 | 实验结论 |
| 取黑色粉末少许,加入过量的 稀盐酸 | 黑色粉末部分溶解,溶液由无色逐渐变为蓝色, | 猜想一和猜想二错误 |
(1)实验中观察到的现象是黑色粉末变红色,澄清石灰水变浑浊,写出两种黑色粉末发生反应的化学方程式2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
(2)小红同学认为该装置设计存在问题,你认为该装置缺陷后是没有尾气处理,若产生的气体中含有一氧化碳会污染空气.
19.用Y形管可进行多种实验.
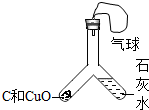
(1)实验一:用酒精喷灯加热左边管内固体,观察到黑色固体变红色;澄清石灰水变浑浊,该Y形管内发生反应的化学方程式为C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;CO2+Ca(OH)2=CaCO3↓+H2O.
(2)实验二:实验过程中可观察到的现象是上面为蓝色粉末变白,下面为白色粉末变蓝,其中发生分解反应的化学方程式为CuSO4•5H2O$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+5H2O;
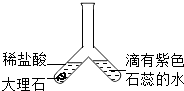
(3)实验三:实验开始1分钟后,右边管内液体变红,该实验所体现的二氧化碳的性质是(用化学方程式表示)CO2+H2O=H2CO3.
| 实验一 | 实验二 | 实验三 |
 | 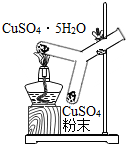 |  |
(2)实验二:实验过程中可观察到的现象是上面为蓝色粉末变白,下面为白色粉末变蓝,其中发生分解反应的化学方程式为CuSO4•5H2O$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+5H2O;
(3)实验三:实验开始1分钟后,右边管内液体变红,该实验所体现的二氧化碳的性质是(用化学方程式表示)CO2+H2O=H2CO3.