题目内容
7.小明参观生态农庄后,对化学在生态农业方面的作用有了深入的了解,以下是他的总结.(1)农作物生长对土壤酸碱度有一定的要求,常用pH试纸测定土壤的酸碱度.有些酸性土壤需要改良,通常给土壤施用D(填序号),既能改良酸性土壤又能给土壤施肥.
A.生石灰 B.熟石灰 C.磷酸钙D.草木灰(主要成分碳酸钾)
(2)农民常在塑料大棚的上方悬挂一些炭火盆,生成的二氧化碳可作气体肥料促进光合作用,使农作物增产.
(3)合理施用化肥可增加粮食产量,常用的化肥有K2SO4、CO(NH2)2、Ca(H2PO4)2、KNO3等,其中属于复合肥的是KNO3,如将尿素与熟石灰研磨不能(填“能”、“不能”)产生氨气;
(4)生态农庄大量用沼气作能源,沼气的主要成分是CH4(填化学式),沼气燃烧产生的光和热可用于做饭、照明、取暖等,从环境保护的角度考虑,在煤气、天然气和氢气中,首选的燃料是氢气.
分析 (1)用pH试纸可以测定溶液的酸碱性;
(2)二氧化碳可作气体肥料促进光合作用,
(3)含有钾元素的化肥属于钾肥;含有磷元素的化肥属于磷肥.
(4)沼气的主要成分是甲烷,氢气燃烧只生成水,热值高,是理想的燃料.
解答 解:(1)农作物生长对土壤酸碱度有一定的要求,常用pH试纸测定土壤的酸碱度.根据信息“既可用来改良土壤酸性,又能给土壤施肥”知,所选物质显碱性且含有氮、磷、钾中的至少一种元素,所以为草木灰(主要成分碳酸钾).故填:pH试纸.D.
(2)农民常在塑料大棚的上方悬挂一些炭火盆,生成的二氧化碳可作气体肥料促进 光合作用,使农作物增产;故答案为:光合;
(3)硫酸钾含有钾元素,属于钾肥;磷酸二氢钙含有磷元素,属于磷肥;尿素不是铵态氮肥,不能与熟石灰研磨产生氨气.故填:KNO3.不能;
(4)沼气的主要成分是甲烷,甲烷燃烧能生成二氧化碳和水,从环境角度考虑,煤气、天然气燃烧都生成二氧化碳,二氧化碳是一种温室气体,大气中二氧化碳的含量过高时,会导致温室效应;
氢气燃烧只生成水,不污染环境,是最理想的燃料.故填:CH4;氢气.
点评 本题考查了化学与生活的知识,完成此题,可以依据已有的知识结合题干提供的信息进行.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
20.自然灾害的频发足以毁灭我们的家园,灾害中常有如下现象发生,其中属于化学变化的是( )
| A. | 冰雪融化 | B. | 房屋倒塌 | C. | 火山喷发 | D. | 山体滑坡 |
2. 如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中正确的是( )
如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中正确的是( )
 如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中正确的是( )
如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中正确的是( )| A. | 该实验证明空气中氧气的含量约占总质量的$\frac{1}{5}$ | |
| B. | 实验时红磷一定要过量 | |
| C. | 可用硫或木炭代替红磷完成实验 | |
| D. | 红磷燃烧产生大量的白雾,火焰熄灭后立刻打开弹簧夹 |
19.下列物质不属于纯净物的是( )
| A. | 冰水混合物 | |
| B. | 二氧化碳 | |
| C. | 液氧 | |
| D. | 氯酸钾和二氧化锰充分加热后的残余固体 |
16.如图所示实验操作,正确的是( )
| A. |  振荡试管 | B. |  取用液体 | ||
| C. |  放置洗过的试管 | D. |  塞紧试管 |
15.根据下列实验要求回答问题.

(1)制取气体前应先检查装置的气密性,若按如图1操作,结构在导管口未看到气泡,其可能原因与下列因素无关的是ab(填序号).
a.将烧杯换成水槽
b.导管伸入水中位置过深,气体无法逸出
c.先用手捂住试管壁,再将导管另一端插入水中
(2)写出图1中仪器的名称:①试管;②集气瓶.
(3)实验室若需要在常温下制取氧气,可以选用(从A-E)的装置组合有BC或BE;若用E装置收集气体时.开始在气泡连续均匀冒出时将导管伸入集气瓶中.写出该反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;若需要用该反应获得比较平稳的氧气流,你的建议是将长颈漏斗换成分液漏斗.
(4)若进一步对常温下该反应进行如下研究,实验记录如下:
有学生认为收集相同体积氧气应用E装置,理由是容易判断集气瓶中的氧气是否收集满;从实验数据可知,本实验中二氧化锰粉末的最佳用量是C.
A.0.3g B.0.5g C.0.7g D.0.9g
(5)若需要用水将F装置中收集好的氧气从瓶内排出,水须从b(填“a”或“b”)端导管口通入.
(6)实验室若用A装置制取0.96克氧气,则至少需要分解0.02摩尔的氯酸钾固体?

(1)制取气体前应先检查装置的气密性,若按如图1操作,结构在导管口未看到气泡,其可能原因与下列因素无关的是ab(填序号).
a.将烧杯换成水槽
b.导管伸入水中位置过深,气体无法逸出
c.先用手捂住试管壁,再将导管另一端插入水中
(2)写出图1中仪器的名称:①试管;②集气瓶.
(3)实验室若需要在常温下制取氧气,可以选用(从A-E)的装置组合有BC或BE;若用E装置收集气体时.开始在气泡连续均匀冒出时将导管伸入集气瓶中.写出该反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;若需要用该反应获得比较平稳的氧气流,你的建议是将长颈漏斗换成分液漏斗.
(4)若进一步对常温下该反应进行如下研究,实验记录如下:
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 |
| 10%过氧化氢溶液的用量/mL | 30 | 30 | 30 | 30 | 30 | 30 |
| 二氧化锰粉末的用量/g | 0.1 | 0.3 | 0.5 | 0.7 | 0.9 | 1.1 |
| 收集相同体积氧气时所用的时间/s | 17 | 7 | 4 | 2 | 2 | 2 |
A.0.3g B.0.5g C.0.7g D.0.9g
(5)若需要用水将F装置中收集好的氧气从瓶内排出,水须从b(填“a”或“b”)端导管口通入.
(6)实验室若用A装置制取0.96克氧气,则至少需要分解0.02摩尔的氯酸钾固体?

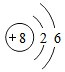 ;⑦核电荷数为12的金属离子Mg2+;⑧保持氢气化学性质的最小粒子H2.
;⑦核电荷数为12的金属离子Mg2+;⑧保持氢气化学性质的最小粒子H2. 向CuSO4和H2SO4的混合溶液中,逐滴加入NaOH溶液.滴加NaOH溶液的质量与生成沉淀的质量关系如图,结合如图回答问题:
向CuSO4和H2SO4的混合溶液中,逐滴加入NaOH溶液.滴加NaOH溶液的质量与生成沉淀的质量关系如图,结合如图回答问题: