题目内容
10. 化学兴趣小组同学为测定某赤铁矿石中氧化铁的质量分数,进行了以下实验:
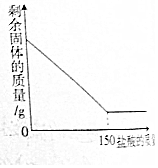
化学兴趣小组同学为测定某赤铁矿石中氧化铁的质量分数,进行了以下实验:Ⅰ.甲同学取该赤铁矿石样品10g,逐滴加入溶质质量分数为7.3%的稀盐酸,剩余固体的质量与加入稀盐酸的质量关系如图所示(杂质既不溶于水也不溶于酸)
(1)甲同学实验过程中的现象是红色固体逐渐溶解,溶液由无色逐渐变成黄色;
(2)赤铁矿石中铁的质量分数是多少?(写出计算过程)
分析 根据氧化铁与稀盐酸的反应分析反应的现象,由剩余固体的质量与加入稀盐酸的质量关系图分析反应稀盐酸的质量,由盐酸中溶质的质量求出氧化铁的质量,再求出赤铁矿石中铁的质量分数.
解答 解:(1)由于氧化铁能与稀盐酸反应生成了氯化铁和水,所以甲同学实验过程中的现象是:红色固体逐渐溶解,溶液由无色逐渐变成黄色;
(2)设赤铁矿石中氧化铁的质量为x
Fe2O3+6HCl=2FeCl3+3H2O
160 219
x 150g×7.3%
$\frac{160}{219}=\frac{x}{150g×7.3%}$ 解得:x=8g
赤铁矿石中铁的质量分数是:$\frac{8g×\frac{112}{160}×100%}{10g}×100%$=56%
故答为:(1)红色固体逐渐溶解,溶液由无色逐渐变成黄色;(2)赤铁矿石中铁的质量分数是56%.
点评 本题主要考查了根据化学方程式的计算,根据剩余固体的质量与加入稀盐酸的质量关系图找出参加反应的稀盐酸的质量是解答本题的关键

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
20.下列说法不正确的是( )
| A. | 石墨具有金属光泽,能导电、导热,但是石墨一种非金属材料 | |
| B. | 食物淀粉在人体内经酶的催化作用,与水发生一系列反应,最终可以变成葡萄糖 | |
| C. | 为了加快电解水的速度,可以向水中加入少量的硫酸钠,硫酸钠在实验中能增强水的导电性 | |
| D. | 生石灰具有吸水性,它能干燥N2、O2、CO2、NH3气体 |
1.如图所示的是甲、乙、丙三种物质的溶解度曲线图,下列说法中,正确的是( )
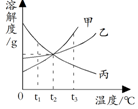

| A. | 0℃时,在甲、乙、丙三种物质中,丙物质形成的溶液的溶质质量分数最大 | |
| B. | 将t1℃时的甲的饱和溶液降温,会使它变成不饱和溶液 | |
| C. | t2℃时,甲、乙、丙三种物质的溶解度相同 | |
| D. | 将t3℃时乙的接近饱和的溶液升温,会使它变成饱和溶液 |
18.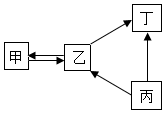 甲、乙、丙、丁均为初中化学常见物质,它们之间的部分转化关系如图所示.下列说法正确的是( )
甲、乙、丙、丁均为初中化学常见物质,它们之间的部分转化关系如图所示.下列说法正确的是( )
 甲、乙、丙、丁均为初中化学常见物质,它们之间的部分转化关系如图所示.下列说法正确的是( )
甲、乙、丙、丁均为初中化学常见物质,它们之间的部分转化关系如图所示.下列说法正确的是( )| A. | 若甲、乙、丁都是氧化物,则丙可能是碳酸钙 | |
| B. | 若丙是碳酸钠,乙是氢氧化钠,则甲可能是硝酸钠 | |
| C. | 若甲、乙、丙、丁均含有同一种元素,且乙可用来灭火,则丙可能是氧气 | |
| D. | 甲、乙、丙、丁之间的转化不可以全部通过复分解反应实现 |
5.向35.0g K2CO3和Na2CO3混合物中,加入一定量10.95%稀盐酸恰好完全反应,对所得溶液进行蒸发,干燥,称量,得固体38.3g,将生成的气体全部通入足量的澄清石灰水中,产生m g沉淀,下列说法正确的是( )
| A. | 蒸发过程中用到的仪器有蒸发皿、酒精灯、玻璃棒、量筒等 | |
| B. | 实验过程中产生的CO2为8.8g | |
| C. | 所用盐酸的质量为200g | |
| D. | 如用10.95%的稀盐酸将m g沉淀溶解,则所用稀盐酸的量与题中的一定量不相等 |
15.除去下列物质中的少量杂质,所选用的试剂、操作方法都正确的是( )
| 选项 | 物质 | 杂质 | 试剂 | 操作方法 |
| A | MnO2 | KCl | 适量水 | 溶解、过滤、洗涤、干燥 |
| B | O2 | H2O | 浓硫酸 | 通过盛有浓硫酸的洗气瓶 |
| C | CaO | CaCO3 | 稀盐酸 | 过滤、蒸发结晶 |
| D | NaOH | Ca(OH)2 | 过量Na2CO3溶液 | 溶解、过滤、蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
2.下列实验操作正确的是( )
| A. | 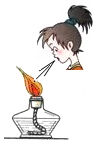 熄灭酒精灯 | B. | 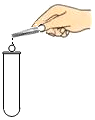 取用大理石块 | C. | 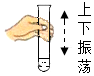 振荡试管 | D. |  闻气味 |
20.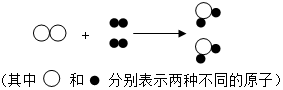 如图表示在一定条件下发生某化学反应的微观过程,则下列说法正确的是( )
如图表示在一定条件下发生某化学反应的微观过程,则下列说法正确的是( )
 如图表示在一定条件下发生某化学反应的微观过程,则下列说法正确的是( )
如图表示在一定条件下发生某化学反应的微观过程,则下列说法正确的是( )| A. | 两物质反应物均为化合物 | B. | 该反应属于置换反应 | ||
| C. | 该反应不符合质量守恒定律 | D. | 化学反应前后元素种类不变 |
 2016年2月4日,国务院发布了《关于钢铁行业化解过剩产能,实现脱困发展的意见》,推动钢铁行业升级.钢铁是一种重要的金属材料.
2016年2月4日,国务院发布了《关于钢铁行业化解过剩产能,实现脱困发展的意见》,推动钢铁行业升级.钢铁是一种重要的金属材料.