题目内容
20. 水是一种重要的资源.
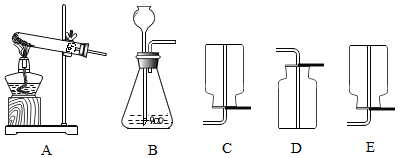
水是一种重要的资源.(1)电解水实验揭示了水的组成(如图 1),其化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,该过程中原子的数目不变(填“减少”“不变”或“增多”).
图 1 中得到氢气的试管是1(填“1”或“2”),电解水时加入少量的 NaOH 溶液的目的是增强水的导电性.
(2)图 2 为太阳能海水淡化装置示意图.
①水变成水蒸气的过程中,不发生变化的是ab(填序号).
a.分子质量b.分子种类c.分子间隔
②利用该装置将一定量的海水暴晒一段时间后,剩余海水中氯化钠的质量分数会变大(填“变大”“变小”或“不变”).
(3)用水灭火时,将水喷成 细雾状的主要原因是b(填序号).
a.降低着火点 b.增大与可燃物接触面积c.与空气中气体反应生成 CO2.
(4)在生活中区分硬水和软水可用肥皂水(填试剂名称).
分析 (1)根据电解水试验的现象、结论及注意事项等分析回答有关的问题;
(2)根据利用太阳能海水淡化的过程中微粒的变化和溶质质量分数的计算公式分析;
(3)根据灭火的方法分析回答;
(4)根据生活中区分硬水和软水的方法分析回答.
解答 解:(1)电解水生成了氢气和氧气,其化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,该过程中原子的数目不变;图1中试管1得到的气体是电源的负极产生的气体是氢气,电解水时加入少量的 NaOH 溶液的目的是增强水的导电性.
(2)①水变成水蒸气的过程中,不发生变化的是分子的质量和分子的种类,分子的间隔变大了.
②利用该装置将一定量的海水暴晒一段时间后,水的质量减少了,氯化钠的质量不变,所以太阳能海水淡化剩余海水中氯化钠的质量分数会变大.
(3)用水灭火时,将水喷成 细雾状的主要原因是增大与可燃物接触面积;
(4)在生活中区分硬水和软水可用肥皂水,遇肥皂水产生的泡沫少的是硬水,遇肥皂水产生的泡沫多的是软水.
故答为:(1)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;不变;1;增强水的导电性.(2)ab;变大;(3)b;(4)肥皂水.
点评 本题主要考查了水的组成、净化、应用以及硬水和软水的区分等知识,属于课本中的基础知识,根据已有的知识分析解答即可.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
11.请将下列物质按要求分类:
(1)a.蒸馏水 b.镁条 c.水银 d.碳酸氢钠 e.氢氧化钡溶液 f.碘
属于单质的是bcf;属于氧化物的是a;属于化合物的是ad;属于混合物的是e.
(2)在一密闭容器中有M、N、P、Q四种物质,在一定条件下使之充分反应后,测得反应前后各物质的质量如下表所示:
①该反应的基本反应类型为B(请填序号);
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
②N的待测值为18g.
(1)a.蒸馏水 b.镁条 c.水银 d.碳酸氢钠 e.氢氧化钡溶液 f.碘
属于单质的是bcf;属于氧化物的是a;属于化合物的是ad;属于混合物的是e.
(2)在一密闭容器中有M、N、P、Q四种物质,在一定条件下使之充分反应后,测得反应前后各物质的质量如下表所示:
| 物质 | M | N | P | Q |
| 反应前的质量/g | 80 | 1 | 1 | 1 |
| 反应前的质量/g | 1 | 待测 | 45 | 19 |
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
②N的待测值为18g.
8.下表列出了除去物质中所含少量杂质的方法,其中正确的是( )
| 物 质 | 所含杂质 | 除去杂质的方法 | |
| A | CO2气体 | CO | 点燃 |
| B | KClO3 | KCl | 加热至不再产生气体 |
| C | Fe粉 | Cu粉 | 加入足量稀硫酸,充分反应,过滤 |
| D | FeSO4溶液 | CuSO4 | 加入足量铁粉,充分反应,过滤 |
| A. | A | B. | B | C. | C | D. | D |
5.如图是某化学反应的微观模型,下列各项中对图示模型理解正确的是( )


| A. | 该反应属于分解反应 | |
| B. | 反应物和生成物中只有一种单质 | |
| C. | 反应中共有两种元素参与 | |
| D. | 参加反应的两种物质分子个数比为2:3 |
10.稀盐酸和稀硫酸具有许多相似化学性质的原因是( )
| A. | 他们都是溶液 | B. | 它们都含有酸根离子 | ||
| C. | 它们都含有氢元素 | D. | 它们的溶液中都含氢离子 |