题目内容
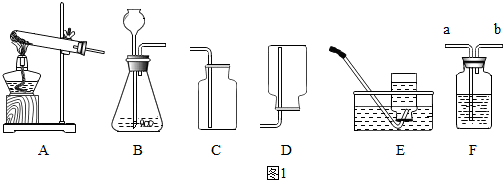
实验室制取CO2,应选用的药品是( )
| A、碳酸钙和稀盐酸 |
| B、木炭和氧气 |
| C、大理石和稀盐酸 |
| D、高温煅烧石灰石 |
考点:二氧化碳的实验室制法
专题:常见气体的实验室制法、检验、干燥与净化
分析:A、考虑碳酸钙和稀盐酸,制取二氧化碳;
B、用木炭和氧气反应生成二氧化碳,操作繁琐,不易收集;
C、大理石和稀盐酸反应速率适中,便于收集二氧化碳.
D、高温煅烧石灰石在实验室里不易达到高温煅烧的条件;
B、用木炭和氧气反应生成二氧化碳,操作繁琐,不易收集;
C、大理石和稀盐酸反应速率适中,便于收集二氧化碳.
D、高温煅烧石灰石在实验室里不易达到高温煅烧的条件;
解答:解:A、碳酸钙和稀盐酸生成二氧化碳;故A正确;
B、木炭和氧气虽然可以生成二氧化碳,但效率低且生成的二氧化碳不易分离出来;故B不正确;
C、大理石和稀盐酸反应速率适中,原料易得,价格便宜,所以实验室制取二氧化碳通常选用大理石和稀盐酸;故C正确.
D、高温煅烧石灰石在实验室里不易达到高温煅烧的条件;故D不正确.
故选AC.
B、木炭和氧气虽然可以生成二氧化碳,但效率低且生成的二氧化碳不易分离出来;故B不正确;
C、大理石和稀盐酸反应速率适中,原料易得,价格便宜,所以实验室制取二氧化碳通常选用大理石和稀盐酸;故C正确.
D、高温煅烧石灰石在实验室里不易达到高温煅烧的条件;故D不正确.
故选AC.
点评:制取气体选择药品时,既要分析反应能否进行,又要分析反应条件是否容易达到,生成的气体是否容易达到、反应速率的快慢等因素,在综合了各种因素后,才会找到最为合理的制取方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列化学与含义相符的是( )
| A、2O-----2个氧元素 |
| B、P2O5----五氧化二磷 |
| C、H2-----2个氢原子 |
| D、Ca-----钙离子 |
据《2013-2017年中国天然气产业供需预测与投资战略分析报告》显示,从2010年到2050年,世界能源需求将增加60%,但煤炭和石油消费将处于逐步下降趋势,到2040年天然气的比例将与石油持平,到2050年将超过石油,成为世界第一能源.天然气的主要成分是( )
| A、氢气 | B、一氧化碳 |
| C、甲烷 | D、氧气 |
粗食盐的杂质主要是MgCl2,工业上常把粗盐晶体粉碎后用饱和食盐水浸洗,再滤出食盐.对此,下列有关说法正确的是( )
| A、浸洗前后,被浸洗的食盐中MgCl2的含量不变 |
| B、浸洗前后,食盐水中NaCl的质量不变 |
| C、浸洗用的饱和食盐水可以无限次的使用 |
| D、粗盐粉碎的颗粒大小不影响浸洗后盐中MgCl2的含量 |


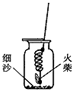 做完“铁在氧气里燃烧”实验后,某兴趣小组有一些疑惑不解的问题,于是他们进行了以下探究活动,请你一同参与.
做完“铁在氧气里燃烧”实验后,某兴趣小组有一些疑惑不解的问题,于是他们进行了以下探究活动,请你一同参与.