题目内容
核电荷数为1~18的元素的原子结构示意图等信息如下,回答下列问题:
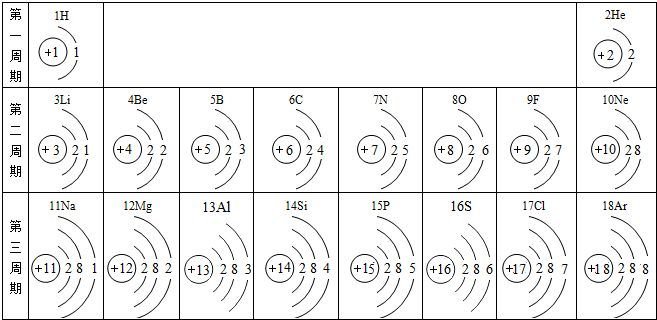
(1)在第二周期中,各原子结构的共同之处是 ;该周期中,各原子核外电子排布的变化规律是 .
(2)在第三周期中,元素类型的变化情况是:从左到右由 元素过渡到 元素,并以稀有气体元素结束.
(3)写出一个核外电子排布与氖原子相同的阳离子:阳离子 .

(1)在第二周期中,各原子结构的共同之处是
(2)在第三周期中,元素类型的变化情况是:从左到右由
(3)写出一个核外电子排布与氖原子相同的阳离子:阳离子
考点:元素周期表的特点及其应用,原子结构示意图与离子结构示意图
专题:化学用语和质量守恒定律
分析:(1)根据元素周期数与电子层数的关系、同一周期原子核外电子排布的变化进行分析解答.
(2)根据在第三周期中,元素类型的变化情况是:从左到右由金属元素过渡到非金属元素,并以稀有气体元素结束进行解答;
(3)根据核外电子排布与与氖原子相同的阳离子可能是钠离子或镁离子以及铝离子等进行解答.
(2)根据在第三周期中,元素类型的变化情况是:从左到右由金属元素过渡到非金属元素,并以稀有气体元素结束进行解答;
(3)根据核外电子排布与与氖原子相同的阳离子可能是钠离子或镁离子以及铝离子等进行解答.
解答:解:(1)在第二周期中,各原子结构的共同之处是原子核外电子层数相同;该周期中,从左到右,各原子核外电子排布的变化规律是最外层电子数依次增加;
(2)在第三周期中,元素类型的变化情况是:从左到右由金属元素过渡到非金属元素,并以稀有气体元素结束;
(3)核外电子排布与与氖原子相同的阳离子可能是钠离子或镁离子以及铝离子,离子符号分别为Na+、Mg2+、Al3+.
故填:(1)各原子的电子层数相同;最外层电子数依次递增;
(2)金属;非金属;
(3)Na+(或Mg2+、Al3+).
(2)在第三周期中,元素类型的变化情况是:从左到右由金属元素过渡到非金属元素,并以稀有气体元素结束;
(3)核外电子排布与与氖原子相同的阳离子可能是钠离子或镁离子以及铝离子,离子符号分别为Na+、Mg2+、Al3+.
故填:(1)各原子的电子层数相同;最外层电子数依次递增;
(2)金属;非金属;
(3)Na+(或Mg2+、Al3+).
点评:本题难度不大,考查学生灵活运用元素周期表中元素的信息、了解原子结构示意图的意义进行分析解题的能力.

练习册系列答案
相关题目
下列物质属于混合物的是( )
| A、冰水混合物 | B、洁净的空气 |
| C、二氧化碳 | D、铝箔 |
碘酸钠放在食盐里可预防碘缺乏症,其中碘元素是+5价,它的化学式是( )
| A、NaIO3 |
| B、NaIO4 |
| C、NaIO2 |
| D、NaI |
河北省境内有一座著名的龙泉寺,泉水常年流淌不断,经测定泉水中含有人体所需的多种矿物质,其物质组成中所含的锌、钙、锶是指( )
| A、原子 | B、分子 | C、离子 | D、元素 |

 ,试回答:
,试回答: 我们知道水既普通又宝贵,日常生活、工农业生产和科学研究都离不开水,通过电解水实验探究水的元素组成.
我们知道水既普通又宝贵,日常生活、工农业生产和科学研究都离不开水,通过电解水实验探究水的元素组成.