题目内容
7.如图是实验室制取气体的常用装置,请回答下列问题: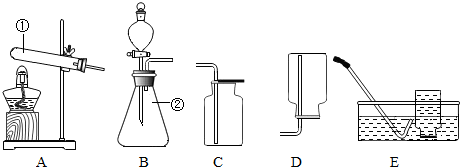
(1)写出图中标号仪器的名称:①试管;②锥形瓶.
(2)实验室可加热KClO3和MnO2的固体混合物制取氧气,请写出该反应的化学方程式:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,应选择的气体发生装置是A(填字母,下同).若用向上排空气法收集氧气,验满的方法是:将带火星的木条放在集气瓶口,若复燃,则证明氧气已满.
(3)实验室可用Zn粒和稀硫酸制取氢气,请写出该反应的化学方程式:Zn+H2SO4═ZnSO4+H2↑,应选择的气体发生装置是B.
(4)常温下,乙烯(C2H4)是一种无色气体,密度与空气相近,难溶于水,不与空气和水发生反应.实验室收集乙烯时,应选择的装置是E.
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
(2)氯酸钾在二氧化锰的催化作用下,受热分解生成氯化钾和氧气;氧气能够支持燃烧,能使带火星的木条复燃;
(3)通常情况下,锌和稀硫酸反应生成硫酸锌和氢气,氢气难溶于水,密度比空气小;
(4)根据气体的性质可以选择收集装置.
解答 解:(1)①是试管,常用作反应容器;②是锥形瓶,常用作反应容器.
故填:试管;锥形瓶.
(2)实验室利用KClO3和MnO2的固体混合物制取氧气需要加热,应该用A装置作为发生装置;
请该反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
若用向上排空气法收集氧气,验满的方法是:将带火星的木条放在集气瓶口,若复燃,则证明氧气已满.
故填:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;A;带火星的木条.
(3)实验室用Zn粒和稀硫酸制取氢气反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑;
锌和稀硫酸反应不需要加热,应选择的气体发生装置是B.
故填:Zn+H2SO4═ZnSO4+H2↑;B.
(4)常温下,乙烯的密度与空气相近,不能用排空气法收集,乙烯难溶于水,不与水发生反应,因此实验室收集乙烯时,可以用排水法收集,即用E装置收集.
故填:E.
点评 本题主要考查仪器的用途、反应表达式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.

练习册系列答案
 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
12.下列物质中属于纯净物的是( )
| A. | 空气 | B. | 澄清石灰水 | C. | 一氧化碳 | D. | 碘酒 |
16.化学研究的对象是物质,它主要是研究物质的组成、结构、性质和变化规律.取一块食盐可以从不同的角度进行研究,以下不是化学研究领域的是( )
| A. | 食盐是由什么成分组成 | B. | 食盐有什么性质和用途 | ||
| C. | 食盐的微观结构如何 | D. | 食盐的产地在哪里 |
15.下列实验操作中,说法错误的是( )
| A. | 向酒精灯内添加的酒精量不能超过酒精灯容积的$\frac{2}{3}$ | |
| B. | 给试管中的液体加热,试管中的液体不能超过试管容积的$\frac{1}{3}$ | |
| C. | 没说明药品的用量时应取最少量,即液体2-3mL,固体1药匙 | |
| D. | 取85mL液体,需要100mL量筒和滴管 |