题目内容
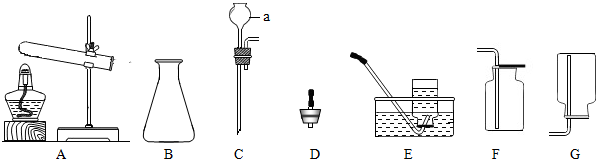
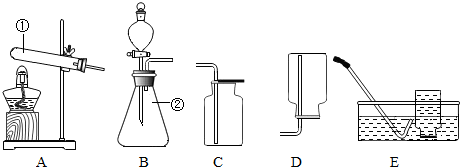
19.实验室常用下列装置来制取氧气:
(1)写出图中有标号仪器的名称:a酒精灯、b铁架台.
(2)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是B(填序号),其中二氧化锰起催化作用.
(3)用高锰酸钾制取氧气时,应选用的发生装置为A,收集装置C或D用E装置检验氧气是否集满的方法是将带火星的木条靠近集气瓶口,若木条迅速复燃,证明已收集满氧气.
(4)实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小.NH3极易溶于水,其水溶液呈碱性.
①制取氨气反应的方程式:2NH4Cl+Ca(OH)2═CaCl2+2NH3↑+2X.
X的化学式为:H2O.
②NH3是一种碱性气体,干燥时不能选用下列干燥剂中的B(填序号).
A.固体氢氧化钠 B.浓硫酸 C.生石灰.
分析 (1)(1)要熟悉各种仪器的名称、用途和使用方法;
(2)根据双氧水是液体,二氧化锰是固体,也就是固液常温下的反应,选择发生装置;
(3)根据如果用高锰酸钾就需要加热解答,根据氧气能够支持燃烧,能使带火星的木条复燃.
(4)
①根据质量守恒定律的实质分析;
②根据氨气为碱性的物质,所以该物质的干燥剂为碱性,故可以据此解答该题.
解答 解:
(1)a是酒精灯; b铁架台,常用于固定、支持实验装置;
(2)如果用过氧化氢和二氧化锰制氧气,就不需要加热,其中二氧化锰起催化作用.故答案为:B;催化.
(3)用高锰酸钾制氧气就需要加热,属于固固加韧性;氧气的验满方法是:将带火星的木条靠近集气瓶口,若木条迅速复燃,证明已收集满氧气.
(4)①制取氨气反应的方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2X.根据质量守恒定律可以知道反应前后原子的个数相等,反应物中所含的原子的种类和个数为:2N 10H 2Cl Ca 2O,生成物中已知物质中原子的种类和个数为:Ca 2Cl 2N 6H,则两个X分子中含有4个氢原子和2个氧原子,一个X分子中含有2个氢原子和1个氧原子,X的化学式为H2O.故答案为:H2O
②干燥剂所干燥的气体必须不能与干燥剂发生反应,NH3是一种碱性气体,干燥时不能选用浓硫酸,因为浓硫酸能与氨气发生反应,故选B.
答案:
(1)酒精灯 铁架台
(2)B 催化
(3)A C 或 D 将带火星的木条靠近集气瓶口,若木条迅速复燃,证明已收集满氧气
(4)H2O B
点评 解答本题关键是要熟记方程式的书写方法,了解收集到不纯气体的原因,知道发生装置和收集装置的选取方法,知道干燥剂对所干燥的气体的要求.

| A. | N(NO2)3中氮元素和氧元素的原子个数是2:5 | |
| B. | N(NO2)3中氮元素和氧元素的质量比是7:4 | |
| C. | N(NO2)3相对分子质量是152g | |
| D. | N(NO2)3氮元素的质量分数是36.8% |
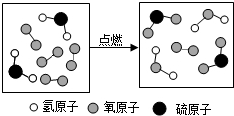 如图是某反应的微观示意图,下列说法不正确的是( )
如图是某反应的微观示意图,下列说法不正确的是( )| A. | 反应物中有单质 | B. | 该反应前后分子个数不变 | ||
| C. | 生成物的分子个数比为1:1 | D. | 参加反应的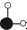 和 和 的质量比为17:24 的质量比为17:24 |
| A. | 白酒和白醋──闻气味 | B. | 铜片和铁片──观察颜色 | ||
| C. | N2和CO2──燃着的木条 | D. | 空气和氧气──带火星的木条 |