题目内容
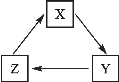
【题目】根据下列粒子结构示意图,回答问题:

(1)上述示意图中,共包含_____种元素。
(2)A、B、C、E中属于阴离子的是_____(填字母序号)。
(3)若D表示某元素的原子,则该粒子在化学变化中容易_____(选填“得到”或去”)电子。
(4)若D为离子,则BD构成的化合物的化学式为_____。
【答案】4 E 得到 NaCl
【解析】
(1)质子数决定元素的种类,上述示意图图1中,共有4种质子数,共包含四种元素,它们之间的本质区别是质子数不同。
(2)核内质子数=核外电子数,属于原子;核内质子数>核外电子数,属于阳离子,核内质子数<核外电子数,属于阴离子;A为氢原子,B为钠离子,C硫原子,E是硫离子,为阴离子;属于阴离子的是E。
(3)若D表示某元素的原子,由于在原子中核内质子数=核外电子数,则m=17-2-8=7,最外层电子数大于4,该粒子在化学变化中容易得到电子。
(4)由结构示意图可知,若D为离子,应为氯离子,化合价为-1价,B为钠离子,化合价为+1价,则BD组成的化合物的化学式为NaCl。

练习册系列答案
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
【题目】2018年5月15日我国第一艘国产航母试海成功, 航母的许多电子原件都采用了黄铜(铜和锌的混合物,且铜不与硫酸反应)。为测定某黄铜中锌的质量分数,化学小组的同学称取20g黄铜粉末于烧杯中,将80g稀硫酸分四次加入,充分反应,测得实验数据如下表:
第一次 | 第二次 | 第三次 | 第四次 | |
加入稀硫酸的质量/g | 20 | 20 | 20 | 20 |
烧杯中剩余物质的质量/g | 39.92 | 59.84 | 79.80 | 99.80 |
(1)黄铜粉末完全反应生成氢气的质量为________。
(2)第三次实验结束后溶液中的溶质为___________。
(3)该黄铜粉末中铜的质量分数是______?(写出计算过程)