题目内容
1.将一定质量的NaCl固体完全溶解于38.5g水中,然后向溶液中加入170g溶质质量分数为10%的AgNO3溶液,恰好完全反应,试求:(1)生成沉淀多少克?
(2)反应后所得溶液中溶质的质量分数.(NaCl+AgNO3═AgCl↓+NaNO3)
分析 (1)根据硝酸银的质量结合方程式计算氯化银的质量;
(2)根据硝酸银的质量结合方程式计算硝酸钠的质量,进一步计算反应后所得溶液中溶质的质量分数;
解答 解:设生成氯化银的质量为x,生成硝酸钠的质量为y,
NaCl+AgNO3═AgCl↓+NaNO3,
170 143.5 85
170g×10% x y
$\frac{170}{170g×10%}$=$\frac{143.5}{x}$=$\frac{85}{y}$
x=14.35g,y=8.5g
反应后所得溶液中溶质的质量分数$\frac{8.5g}{38.5g+170g-14.35g}$×100%=4.38%
答:(1)生成沉淀14.35g
(2)反应后所得溶液中溶质的质量分数4.38%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
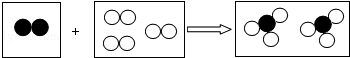
12.如图是某化学反应的微观模型,“ ”、“
”、“ ”分别表示不同元素的原子,下列对图示模型理解正确的是( )
”分别表示不同元素的原子,下列对图示模型理解正确的是( )
 ”、“
”、“ ”分别表示不同元素的原子,下列对图示模型理解正确的是( )
”分别表示不同元素的原子,下列对图示模型理解正确的是( )
| A. | 该反应属于分解反应 | |
| B. | 反应物和生成物中只有一种单质 | |
| C. | 反应中共有两种元素参与,生成物可能为氧化物 | |
| D. | 参加反应的两种物质分子个数之比为2:3 |
9.下列符号中既能代表一种元素,又能代表一种原子,还能代表一种物质的是( )
| A. | Fe | B. | O2 | C. | H | D. | 2H |
16.下列事故处理方法正确的是( )
| A. | 家用电器着火,立即用水浇灭 | |
| B. | 高层住房着火时,立即打开所有门窗 | |
| C. | 发现煤气泄漏时,立即打开抽油烟机 | |
| D. | 炒菜时油锅着火,立即盖上锅盖 |
6.发射神舟六号飞船用的是长征Ⅱ(F)型火箭,该火箭的燃料是偏二甲肼[(CH3)2N-NH2],氧化剂是四氧化二氮(N2O4).下列有关说法正确的是( )
| A. | 在宇宙仓中(失重条件下)比地球上难做过滤实验 | |
| B. | 偏二甲肼由碳原子、氢分子、氮分子组成 | |
| C. | 偏二甲肼由2个碳原子、8个氢原子、2个氮原子构成 | |
| D. | 四氧化二氮组成元素氮、氧的质量比为1:2 |
3.下列各项中不能证明分子之间有间隔的是( )
| A. | 红墨水滴入水中,过一会水全部变成红色 | |
| B. | 水受热变为水蒸气时体积会增大 | |
| C. | 1体积黄豆和1体积小米掺在一起后,总量少于2体积 | |
| D. | 100mL酒精和100mL水混合后,总体积小于200mL |
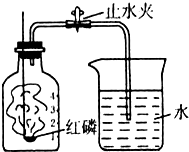 某同学在学习了拉瓦锡测空气中氧气含量的测定方法后,自己设计如图所示的装置,用来测空气中氧气的含量.该同学的实验步骤如下:
某同学在学习了拉瓦锡测空气中氧气含量的测定方法后,自己设计如图所示的装置,用来测空气中氧气的含量.该同学的实验步骤如下: