题目内容
如图为甲、乙两种盐的溶解度曲线,下列说法正确的是( )
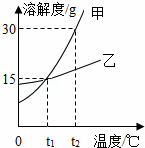
|
| A. | 甲、乙两种物质的溶解度都不相等 |
|
| B. | 将接近饱和的甲溶液变为饱和溶液,可采用蒸发或降温的方法 |
|
| C. | t1℃时,甲、乙两种物质的饱和溶液中,溶质的质量分数均为15% |
|
| D. | t2℃时,将30克乙物质放入100克水中,所得溶液的质量为130克 |
考点:
固体溶解度曲线及其作用;饱和溶液和不饱和溶液相互转变的方法;溶质的质量分数、溶解性和溶解度的关系.
专题:
溶液、浊液与溶解度.
分析:
根据溶解度曲线的意义进行分析解答,交点表示在该温度下两种物质的溶解度相等;溶解度手温度影响变化大的物质,适宜采用降温结晶法析出晶体,受温度影响变化不大的物质,适宜用蒸发结晶法析出晶体,据此解答.
解答:
解:A、溶解度大小比较需要指明具体的温度,故A错误;
B、甲的溶解度随温度升高而增大,故甲的不饱和溶液变为饱和溶液需要蒸发或降温,故B正确;
C、t1℃时,甲、乙两种物质的溶解度相同,所以它们的饱和溶液中,溶质的质量分数均为 ×100%<15%,故C错误;
×100%<15%,故C错误;
D、t2℃时,乙物质的溶解度小于30g,此温度下,将30克乙物质放入100克水中,所得溶液的质量小于为130克,故D错误;
故选B.
点评:
本题考查了溶解度曲线的意义和应用,完成此题,可以依据已有的知识进行.

取四份20℃时一定质量的饱和硝酸钾溶液,分别进行如下实验后,所得结论正确的是( )
|
| A. | 保持温度不变,蒸发10g水后,溶液中溶质的质量分数增大 |
|
| B. | 保持温度不变,加入10g硝酸钾后,溶液中溶质的质量分数增大 |
|
| C. | 保持温度不变,蒸发10g水后,硝酸钾的溶解度增大 |
|
| D. | 降温至10℃时,硝酸钾的溶解度减小 |
甲、乙两种物质的溶解度曲线如图所示.下列说法中正确的是( )

|
| A. | t1℃时,甲饱和溶液的溶质质量分数大于乙饱和溶液 |
|
| B. | t2℃时,甲、乙饱和溶液的溶质质量分数都为30% |
|
| C. | t2℃时,甲、乙的饱和溶液分别降温至t1℃,甲溶液饱和,乙溶液不饱和 |
|
| D. | t2℃时,质量相同的甲、乙饱和溶液分别升温至t3℃,为达饱和状态,需加入甲的质量大于乙 |
图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )

|
| A. | 甲物质的溶解度大于乙物质的溶解度 |
|
| B. | 甲中含有少量的乙,可以用蒸发溶剂的方法提纯甲 |
|
| C. | t2℃时,乙饱和溶液中溶质的质量分数一定小于甲饱和溶液中溶质的质量分数 |
|
| D. | t2℃时,将等质量的甲、乙两种物质的溶液分别降温至t1℃,析出晶体的质量甲一定大于乙 |
下列物质属于化合物的是( )
|
| A. | 河水 | B. | 大理石 | C. | 氮气 | D. | 二氧化硫 |
下列化学用语与其所表达的意义一致的是()
|
| A. | Co﹣﹣﹣1个一氧化碳分子 | B. | 3Fe3+﹣﹣﹣3个亚铁离子 |
|
| C. | 2SO42﹣﹣﹣﹣2个硫酸根离子 | D. | 4N2﹣4个氮原子 |

